题目内容
以下结构简式表示一种有机物的结构,关于其性质的叙述不正确的是( )
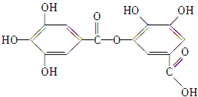

| A、它有酸性,能与纯碱溶液反应 |
| B、可以水解,其水解产物只有一种 |
| C、1 mol该有机物最多能与7 mol NaOH反应 |
| D、该有机物能发生取代反应 |
考点:有机物的结构和性质,有机物分子中的官能团及其结构
专题:有机物的化学性质及推断
分析:由结构简式可知,分子中含酚-OH、-COOH、-COOC-,结合酚、羧酸及酯的性质来解答.
解答:
解:A.含酚-OH、-COOH具有酸性,均能与纯碱溶液反应,故A正确;
B.含-COOC-,可发生水解反应,水解产物只有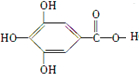 ,故B正确;
,故B正确;
C.5个酚-OH、1个-COOH、1个-COOC-及-COOC-水解生成的酚-OH也与NaOH反应,则1 mol该有机物最多能与8 mol NaOH反应,故C错误;
D.含酚-OH、-COOH,均可发生取代反应,故D正确;
故选C.
B.含-COOC-,可发生水解反应,水解产物只有
 ,故B正确;
,故B正确;C.5个酚-OH、1个-COOH、1个-COOC-及-COOC-水解生成的酚-OH也与NaOH反应,则1 mol该有机物最多能与8 mol NaOH反应,故C错误;
D.含酚-OH、-COOH,均可发生取代反应,故D正确;
故选C.
点评:本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酚、羧酸、酯性的质考查,题目难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
单糖是( )
| A、具有甜味的物质 |
| B、具有一个分子比较简单的糖 |
| C、不能在水解成更简单的糖 |
| D、最简式为的Cn(H2O)m有机物 |
已知分子式为C10H14的分子,不能使溴水褪色,但可使酸化的高锰酸钾溶液褪色.它的分子结构中含有一个烷基,它与液溴在还原铁粉存在下,反应生成物结构有3种,则此烷基的结构有( )
| A、2种 | B、3种 | C、4种 | D、5种 |
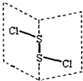 二氯化硫(S2Cl2)广泛用于橡胶工业,分子结构如图.常温下,S2Cl2是一种橙黄色液体,与水迅速反应,并生成能使品红褪色的气体.下列说法正确的是( )
二氯化硫(S2Cl2)广泛用于橡胶工业,分子结构如图.常温下,S2Cl2是一种橙黄色液体,与水迅速反应,并生成能使品红褪色的气体.下列说法正确的是( )A、S2Cl2的电子式: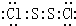 |
| B、S2Cl2为含有极性键和非极性键的非极性分子 |
| C、S2Br2与S2Cl2结构相似,熔沸点:S2Br2<S2Cl2 |
| D、S2Cl2与H2O反应化学方程式可能为:2 S2Cl2+2H2O=SO2↑+3S↓+4HCl |
下列离子中,核外有10个电子的是( )
| A、Mg2+ |
| B、S2- |
| C、K+ |
| D、Cl- |

 的所有原子
的所有原子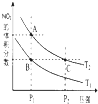 氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.
氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用.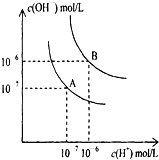 水的电离平衡曲线如图所示.
水的电离平衡曲线如图所示.