��Ŀ����
10������ NaBH4/H2O2ȼ�ϵ�أ�DBFC���Ľṹ��ͼ������֪���⻯������Ϊ-1�ۣ����йظõ�ص�˵����ȷ���ǣ�������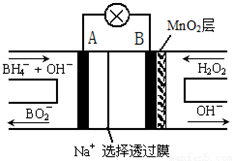
| A�� | �ŵ�����У�����������Һ�е�H+Ũ�ȼ�С | |
| B�� | ����������ĵ缫��ӦΪ��BH${\;}_{4}^{-}$+8OH--8e-=BO$_2^-$+6H2O | |
| C�� | �ŵ�����У�Na+������������Ǩ�� | |
| D�� | �ڵ�ط�Ӧ�У�ÿ����1L 6 mol/LH2O2��Һ��������������·�еĵ���Ϊ6NA�� |
���� �����⻯����NaBH4��BԪ�صĻ��ϼ�Ϊ+3�ۣ���H2O2��ԭ�ϵ�ȼ�ϵ�أ��������Һ�ʼ��ԣ��ɹ���ԭ��װ��ͼ��֪����������������Ӧ���缫��ӦʽΪBH4-+8OH--8e-=BO2-+6H2O������H2O2������ԭ��Ӧ���õ����ӱ���ԭ����OH-���缫��ӦʽΪH2O2+2e-=2OH-���ݴ˷�����
��� �⣺A���ŵ�����У�������H2O2������ԭ��Ӧ���õ����ӱ���ԭ����OH-���缫��ӦʽΪH2O2+2e-=2OH-����������������Һ��OH-��Ũ��������H+Ũ�ȼ�С����A��ȷ��
B����������������Ӧ���缫��ӦʽΪBH4-+8OH--8e-=BO2-+6H2O����B����
C���ŵ�ʱ���������������ƶ�����C����
D���ڵ�ط�Ӧ�У�ÿ����1L 6mol/L H2O2��Һ��������������·�еĵ�����=6mol/L��1L��2��NA/mol=12NA����D����
��ѡA��
���� ���⿼����ԭ���ԭ�����漰�缫��Ӧʽ����д���缫���жϡ������ƶ������֪ʶ�㣬�ѵ��ǵ缫��Ӧʽ����д��Ҫ��ϵ������Һ��д����Ŀ�Ѷ��еȣ������ڿ���ѧ���Ի���֪ʶ���ۺ�Ӧ��������

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
18�����ȷ�Ӧ������һ����Ҫ���ʣ�ijУ��ѧ��ȤС��ͬѧ��ȡ��������������ͼ1ʵ��װ�ý������ȷ�Ӧ����ȴ��õ������顱����
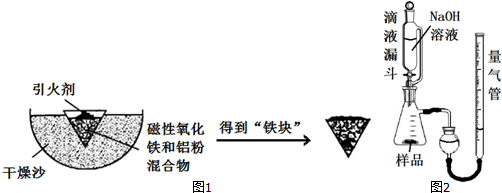
��1��ȡ��Ӧ��ġ����顱����ȡ��������������ͼ2װ�õ�������NaOH��Һ��ַ�Ӧ��������������������Իش��������⣺
�ٸ�ʵ���ʵ��Ŀ���ǣ�������Ʒ�����İٷֺ��������������ƣ���
�������ܵ����߲�����һ����ѧʵ�鳣�����߸�װ���ɣ�������������Ϊ��
���������ڶ���ʱ�������ҹ�Һ����ƽ֮ǰ�IJ����ǻָ������£�
��װ����ʹ�ô�ƽ��ܵĵ�Һ©��������ͨ��Һ©�������˿���ƽ��ѹǿ��Һ��˳��������ƿ֮���������ʵ���������ã����װ��ʹ�÷�Һ©�����������ĸ����ʰٷֺ������ᣨ�ƫ��ƫС������
��2������ȡ�����顱��Ʒ�������ᣬ�����еμ�KSCN��Һ����Һû�г���Ѫ��ɫ��Ϊ�ⶨ��ʵ�����á����顱�ijɷ֣�ʵ��������ͼ3��ʾ��

�����������↑ʼ��������ȫ������pH�����ʾ��
���Լ�AӦѡ��C���Լ�BӦѡ��D��������ţ�
A��ϡ���� B��������C��H2O2��Һ D����ˮ E��MgCO3����
��������ȫ�ı�־��ǰ��������������������0.1g��
�������պ�ɫ��δM������Ϊ12.0g����á����顱�����İٷֺ�����84%��

��1��ȡ��Ӧ��ġ����顱����ȡ��������������ͼ2װ�õ�������NaOH��Һ��ַ�Ӧ��������������������Իش��������⣺
�ٸ�ʵ���ʵ��Ŀ���ǣ�������Ʒ�����İٷֺ��������������ƣ���
�������ܵ����߲�����һ����ѧʵ�鳣�����߸�װ���ɣ�������������Ϊ��
���������ڶ���ʱ�������ҹ�Һ����ƽ֮ǰ�IJ����ǻָ������£�
��װ����ʹ�ô�ƽ��ܵĵ�Һ©��������ͨ��Һ©�������˿���ƽ��ѹǿ��Һ��˳��������ƿ֮���������ʵ���������ã����װ��ʹ�÷�Һ©�����������ĸ����ʰٷֺ������ᣨ�ƫ��ƫС������
��2������ȡ�����顱��Ʒ�������ᣬ�����еμ�KSCN��Һ����Һû�г���Ѫ��ɫ��Ϊ�ⶨ��ʵ�����á����顱�ijɷ֣�ʵ��������ͼ3��ʾ��

�����������↑ʼ��������ȫ������pH�����ʾ��
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| ��ʼ����ʱ��pH | 7.5 | 2.8 | 4.2 | 9.6 |
| ������ȫʱ��pH | 9.0 | 4.0 | 5 | 11 |
A��ϡ���� B��������C��H2O2��Һ D����ˮ E��MgCO3����
��������ȫ�ı�־��ǰ��������������������0.1g��
�������պ�ɫ��δM������Ϊ12.0g����á����顱�����İٷֺ�����84%��
5����NAΪ�����ӵ�������ֵ������������ȷ���ǣ�������
| A�� | 0.1 mol-NH2�к��еĵ�����Ϊ0.7NA | |
| B�� | ��״���£�2.24 L�Ҵ��к��е�C-H��ĿΪ0.5NA | |
| C�� | ���³�ѹ�£�65 g Zn������ŨH2SO4��ַ�Ӧ��ת�Ƶ�����һ��Ϊ2NA | |
| D�� | 2.24 L NO��1.12 L O2��ַ�Ӧ����������ԭ����Ŀһ��Ϊ0.3NA |
2�������£����и�������һ���ܴ���������ǣ�������
| A�� | c��H+��=10-4mol•L-1����Һ�У�NH4+��K+��SO42-��NO3- | |
| B�� | ��ɫ��Һ�У�Na+��Cu2+��Cl-��NO3- | |
| C�� | 0.1 mol•L-1AgNO3 ��Һ��H+��K+��SO42-��I- | |
| D�� | ������ˮ�У�Cl-��Na+��NO3-��SO32- |
19���Ʒ���ʢ�п������ܱ�����������Na2O��Na2O2������������Щ���ؾ����ģ�������
| A�� | ��Ӧ�¶� | B�� | �������� | C�� | �����Ĵ�С | D�� | �Ƶ�״̬ |
20����NAΪ����٤��������ֵ������˵����ȷ���ǣ�������
| A�� | 1mol�����к��е�C-O������ĿΪ2NA | |
| B�� | ��״���£�44.8CHCl3�к��з��ӵ���ĿΪ2NA | |
| C�� | 1 mol-CH3�������ĵ�������Ϊ10 NA | |
| D�� | ��FeI2��Һ��ͨ������Cl2������2 mol Fe2+������ʱ������Cl2�ķ�����ΪNA |
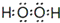 ��
��