题目内容
19.一次区分乙酸、乙醇、苯、四氯化碳四种液体的试剂是( )| A. | H2O | B. | 溴水 | ||
| C. | 新制Cu(OH)2 | D. | 酸性高锰酸钾溶液 |
分析 从水溶性来区分,乙酸和乙醇与水混溶,苯不溶于水,但密度比水小,四氯化碳不溶于水,但密度比水大,在化学性质上乙酸具有酸性,以此解答.
解答 解:A.乙酸、乙醇都溶于水,不能鉴别,故A错误;
B.与A相似,加入溴水,不能鉴别乙酸、乙醇,故B错误;
C.乙酸可溶解氢氧化铜,乙醇溶于水,苯不溶于水,但密度比水小,四氯化碳不溶于水,但密度比水大,可鉴别,故C正确;
D.高锰酸钾可氧化乙醇,溶液褪色,乙酸溶于水,苯不溶于水,但密度比水小,四氯化碳不溶于水,但密度比水大,可鉴别,故D正确.
故选CD.
点评 本题考查有机物的鉴别,题目难度不大,本题注意乙酸、乙醇以及苯的性质的异同,注意乙酸的酸性以及苯、四氯化碳与水互不相溶的性质.

练习册系列答案
相关题目
9.根据表中左栏信息,回答右栏有关问题:
| 信 息 | 问 题 |
| ①短周期元素X、Y、Z、W的原子序数依次增大,它们原子的最外层电子数均不少于最内层电子数.其中X是形成化合物种类最多的元素. | (1)X元素的最高价氧化物的电子式是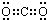 |
| ②在一定条件下,上述四种元素的单质均能与足量的氧气反应,其中Z元素的氧化物既能溶于稀硫酸,又能溶于浓NaOH溶液. | (2)Z元素在元素周期表中位于第 三周期, ⅢA族. |
| ③Y固体单质与盐酸反应,再向反应后的溶液中加入过量的烧碱溶液,最终溶液中有白色沉淀生成. | (3)写出生成白色沉淀的化学方程式 MgCl2+2NaOH═Mg(OH)2↓+2NaCl. |
| ④向上述四种元素的单质的混合物中加入足量的烧碱,固体部分溶解,过滤,向滤液中加入过量 的盐酸溶液,最终溶液中有白色沉淀. | (4)最终生成白色沉淀的离子方程式为 SiO32-+2H+=H2SO3↓. |
| (5)X、Y、Z、W四种元素的原子半径由大到小的顺序为 Mg>Al>Si>C(用元素符号表示) | |
7.下列物质是电解质的为( )
| A. | 硫黄 | B. | 硫酸钠 | C. | 酒精 | D. | 硝酸钾溶液 |
14.下列各有机物在一定的条件下能发生消去反应的是( )
| A. | CH3Cl | B. | (CH3)3CCH2OH | C. | (CH3)3CCl | D. | 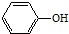 |
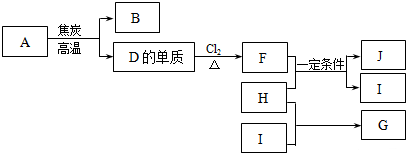
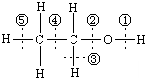 图为乙醇分子的化学键示意图,请按要求回答问题:
图为乙醇分子的化学键示意图,请按要求回答问题: (1)可正确表示原子轨道的是:AC.
(1)可正确表示原子轨道的是:AC.