��Ŀ����
19����һ������þ��ͭ��ɵĻ������뵽ϡ�����У�������ȫ�ܽ⣨���跴Ӧ�л�ԭ����ֻ��NO������Ӧ�����Һ�м���3mol/L NaOH��Һ��������ȫ��������ɳ�����������ԭ�Ͻ����������5.1g��������������ȷ���ǣ�������| A�� | �����ɵij������ﵽ���ʱ������NaOH��Һ�����V��100 mL | |
| B�� | ������ȫ���ܽ�ʱ�ռ���NO��������һ��Ϊ2.24 L | |
| C�� | �μӷ�Ӧ�Ľ�����������3.6 g��m��9.6 g | |
| D�� | ������ȫ���ܽ�ʱ���μӷ�Ӧ����������ʵ���һ����0.4 mol |
���� ��һ������þ��ͭ��ɵĻ������뵽ϡHNO3�У�������ȫ�ܽ⣨���跴Ӧ�л�ԭ����ֻ��NO����������Ӧ��3Mg+8HNO3 ��ϡ��=3Mg��NO3��2+2NO��+4H2O��3Cu+8HNO3 ��ϡ��=3Cu��NO3��2+2NO��+4H2O����Ӧ�����Һ�м��������3mol/L NaOH��Һ��������ȫ��������Ӧ��Mg��NO3��2+2NaOH=Mg��OH��2��+2NaNO3��Cu��NO3��2+2NaOH=Cu��OH��2��+2NaNO3������Ϊ������þ��������ͭ�����ɳ�����������ԭ�Ͻ����������5.1g����������þ��������ͭ����������������Ϊ5.1g�������������ʵ���Ϊ$\frac{5.1g}{17g/mol}$=0.3mol�����ݵ���ת���غ㣬��þ��ͭ���ܵ����ʵ���Ϊ0.15mol��
A��������������ƿ����к�δ��Ӧ�����
B�����ݵ���ת���غ����NO���ʵ�����������岻һ���DZ�״���жϣ�
C�����ü����ٶ�ȫΪþ��ȫΪͭ�����жϣ�
D�����ݷ���ʽ��֪�μӷ�Ӧ��n��Ӧ��HNO3��=$\frac{8}{3}$n����������
��� �⣺��һ������þ��ͭ��ɵĻ������뵽ϡHNO3�У�������ȫ�ܽ⣨���跴Ӧ�л�ԭ����ֻ��NO����������Ӧ��3Mg+8HNO3 ��ϡ��=3Mg��NO3��2+2NO��+4H2O��3Cu+8HNO3 ��ϡ��=3Cu��NO3��2+2NO��+4H2O��
��Ӧ�����Һ�м��������3mol/L NaOH��Һ��������ȫ��������Ӧ��Mg��NO3��2+2NaOH=Mg��OH��2��+2NaNO3��Cu��NO3��2+2NaOH=Cu��OH��2��+2NaNO3������Ϊ������þ��������ͭ�����ɳ�����������ԭ�Ͻ����������5.1g����������þ��������ͭ����������������Ϊ5.1g�������������ʵ���Ϊ$\frac{5.1g}{17g/mol}$=0.3mol�����ݵ���ת���غ㣬��þ��ͭ���ܵ����ʵ���Ϊ0.15mol��
A����������ʣ�࣬��μӷ�Ӧ�������Ƶ����ʵ�������0.3mol����Ҫ����������Һ���=$\frac{0.3mol}{3mol/L}$=0.1L=100mL����������ʣ�࣬���ĵ�����������Һ�������100mL����A��ȷ��
B��þ��ͭ���ܵ����ʵ���Ϊ0.15mol�����ݵ���ת���غ��֪���ɵ�NO���ʵ���Ϊ$\frac{0.15mol��2}{3}$=0.1mol����Ϊ��״���£�����NO�����Ϊ0.1mol��22.4L/mol=2.24L����NO��һ�����ڱ�״�����ռ���NO����������һ��Ϊ2.24L����B����
C��þ��ͭ���ܵ����ʵ���Ϊ0.15mol���ٶ�ȫΪþ������Ϊ0.15mol��24g/mol=3.6g����ȫΪͭ������Ϊ0.15mol��64g/mol=9.6g�����Բμӷ�Ӧ�Ľ�������������m��Ϊ3.6g��m��9.6g����C��ȷ��
D�����ݷ���ʽ��֪�μӷ�Ӧ��n��Ӧ��HNO3��=$\frac{8}{3}$n��������=0.15mol��$\frac{8}{3}$=0.4mol����D��ȷ��
��ѡB��
���� ������Ҫ���������йؼ��㣬�ۺϿ���ѧ���ĵ�ʧ�����غ㡢�����غ���ۺ����úͽ�������������������һ�����������ĺ��⣬�ѶȽϴ�

| A�� | �������ͬλ�� | B�� | ������Ԫ�� | ||
| C�� | ��������ɵ����� | D�� | ��Ԫ�ص����ֲ�ͬ���� |
| A�� | ������������ͺ���շ�Ӧ����ϩʹ���Ը��������Һ����ɫ | |
| B�� | ��ϩ��������Ȼ�̼��Һ��Ӧ������������һ�������·�Ӧ���ɻ����� | |
| C�� | ����Ũ�����Ũ����Ļ��Һ��Ӧ������״Һ�壻��ϩ��ˮ�����Ҵ��ķ�Ӧ | |
| D�� | ��ϩ����ˮ��Ӧ���������Ҵ���������Ӧ |
�й��������↑ʼ�����ͳ�����ȫ��pH���±���
| �������� | Fe��OH��3 | Fe��OH��2 | Cu��OH��2 | Zn��OH��2 |
| ��ʼ����ʱ��pH | 1.9 | 6.5 | 4.2 | 5.4 |
| ��ȫ����ʱ��pH | 3.3 | 9.7 | 6.7 | 8.2 |
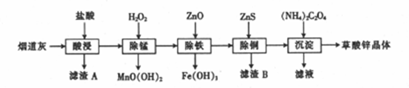
��1������A����Ҫ�ɷ�ΪSiO2���ѧʽ����
��2����������B�����ӷ���ʽΪZnS+Cu2+=CuS+Zn2+��
��3������ʱ����ZnO���Ʒ�ӦҺ��pH��ΧΪ3.3��5.4��
��4������п�������к���H2S������FeCl3��Һ����H2S���õ��������˺�����ʯīΪ�缫����һ�������µ����Һ��
��FeCl3��H2S��Ӧ�����ӷ���ʽΪ2Fe3++H2S=2Fe2++S��+2H+��
�ڵ����������ĵ缫��ӦʽΪ2H+-2e-=H2����
��5��25��ʱ����0.10mol•L-1��H2S��Һ��ͨ��HCl��������NaOH�����Ե�����ҺpH��c��S2-���Ĺ�ϵ��ͼ2��ʾ��������Һ����ı仯��H2S�Ļӷ���
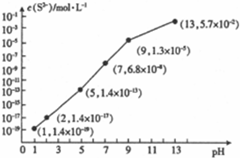
��pH=13ʱ����Һ�е�c��H2S��+c��HS-��=0.043mol•L-1
��ij��Һ�к�δ֪Ũ�ȵ�Mn2+��0.01mol•L-1Fe2+��0.10mol•L-1H2S������ҺpH=2ʱ��Fe2+ ��ʼ��������Mn2+��ʼ����ʱ����Һ��
$\frac{c��M{n}^{2+}��}{c��F{e}^{2+}��}$=2��106��
| A�� | С�մ�--Na2CO3 | B�� | ��ʯ��--Ca ��OH��2 | C�� | ��ȩ--CH3OH | D�� | ����ʯ--CaSO4 |
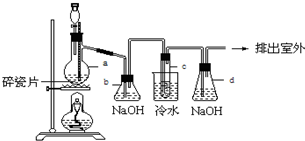
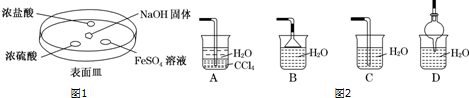
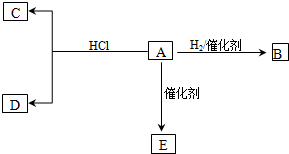

 �ϳ�
�ϳ�  ���������Լ��ͷ�Ӧ��������ȥ����֪DΪ1��3-������ϡ
���������Լ��ͷ�Ӧ��������ȥ����֪DΪ1��3-������ϡ

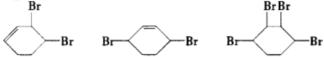 ��
�� ��һ��ͬ���칹��ɷ���������Ӧ��Ҳ����ˮ�⣬�˴Ź���������ʾ�������壬�������Ϊ1��2��9����ͬ���칹��Ľṹ��ʽΪHCOOCH2C��CH3��3
��һ��ͬ���칹��ɷ���������Ӧ��Ҳ����ˮ�⣬�˴Ź���������ʾ�������壬�������Ϊ1��2��9����ͬ���칹��Ľṹ��ʽΪHCOOCH2C��CH3��3 ���л���д�ṹ��ʽ����ע����Ӧ������
���л���д�ṹ��ʽ����ע����Ӧ������