题目内容
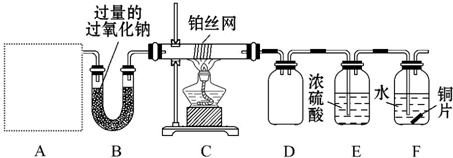
7.氨气在工农业生产中有重要应用,如图1所示,向NaOH固体上滴几滴浓氨水,迅速盖上盖,观察现象.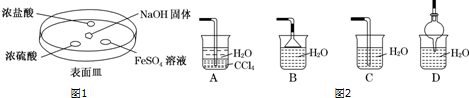
①浓盐酸液滴附近会出现白烟,发生反应的化学方程式为NH3+HCl═NH4Cl.
②FeSO4液滴中先出现灰绿色沉淀,过一段时间后变成红褐色,发生的反应包括Fe2++2NH3•H2O═Fe(OH)2↓+2NH4+和4Fe(OH)2+O2+2H2O═4Fe(OH)3.
(2)已知氨气极易溶于水,而难溶于有机溶剂CCl4.如图2装置中不适宜做氨气尾气吸收的是C.
分析 (1)①浓盐酸和浓氨水易挥发,浓盐酸液滴附近会出现白烟,发生HCl与氨气的反应生成氯化铵;
②氢氧化钠具有吸水性,溶于水并放热,滴加氨水,生成氨气,氨气与浓盐酸反应生成氯化铵,与浓硫酸反应生成硫酸铵或硫酸氢铵,氨气与硫酸亚铁溶液反应生成氢氧化亚铁,氢氧化亚铁不稳定,易被氧化生成氢氧化铁,以此解答;
(2)根据氨气极易溶于水,尾气吸收时要防止倒吸,导气管不能插入到液面以下以及氨气难溶于有机溶剂CCl4.
解答 解:(1)①浓盐酸液滴附近会出现白烟,发生HCl与氨气的反应生成氯化铵,该反应为NH3+HCl═NH4Cl,故答案为:NH3+HCl═NH4Cl;
②FeSO4与碱反应生成白色沉淀,发生反应为Fe2++2NH3•H2O═Fe(OH)2↓+2NH4+,然后出现灰绿色沉淀,过一段时间后变成红褐色,是因氢氧化亚铁被氧化,发生反应为4Fe(OH)2+O2+2H2O═4Fe(OH)3,
故答案为:4Fe(OH)2+O2+2H2O═4Fe(OH)3;
(2)A、水的密度比四氯化碳小,浮在四氯化碳的上面,四氯化碳不能和氨气反应,也不溶解氨气,该装置既能够吸收易溶性气体,又能够防止倒吸.故A正确;
B、吸收装置中的导管下连漏斗,漏斗的边缘紧靠液面,易吸收易溶性气体,能防止倒吸,故B正确;
C、吸收装置中的导气管插入到液面,易吸收易溶性气体,但产生倒吸,故C错误;
D、吸收装置中的导管没直接伸入到液体中,而是与烧杯连接紧密,易吸收易溶性气体,能防止倒吸,故D正确;
故选:C.
点评 本题以氨气的性质考查物质之间的反应,防倒吸装置的原理分析,为高频考点,侧重学生分析能力的考查,注意知识的迁移应用,题目较为基础.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.已知115号元素的一种核素为289X,下列有关叙述正确的是( )
| A. | 115号元素可显+5价 | B. | X原子的中子数与电子数之差为174 | ||
| C. | 115号元素位于周期表第八周期 | D. | 115号元素属于非金属元素 |
19.将一定量的镁和铜组成的混合物加入到稀硝酸中,金属完全溶解(假设反应中还原产物只有NO).向反应后的溶液中加入3mol/L NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g.下列叙述不正确的是( )
| A. | 当生成的沉淀量达到最大时,消耗NaOH溶液的体积V≥100 mL | |
| B. | 当金属全部溶解时收集到NO气体的体积一定为2.24 L | |
| C. | 参加反应的金属的总质量3.6 g<m<9.6 g | |
| D. | 当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4 mol |
16. 已知:①抗坏血酸(C6H8O6)(Vc)溶于水和乙醇,具有抗氧化性,可使酸性高锰酸钾溶液褪色;
已知:①抗坏血酸(C6H8O6)(Vc)溶于水和乙醇,具有抗氧化性,可使酸性高锰酸钾溶液褪色;
②磷酸亚铁[Fe3(PO4)2•8H2O]为白蓝色单斜晶体,溶于稀酸,不溶于水、乙醇、醋酸.
I.磷酸亚铁是生产LiFePO4电池的原料,实验室利用FeSO4•7H2O、Na2HPO4•12H2O及CH3COONa•3H2O为原料制备磷酸亚铁晶体,合成时的主要反应为:
3FeSO4+2Na2HPO4+2CH3COONa+8H2O=Fe3(PO4)2•8H2O↓+3Na2SO4+2CH3COOH
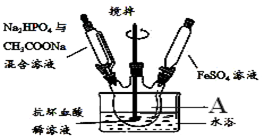
装置如图所示:
实验步骤:
①在50mL干净的仪器A中加入抗坏血酸(C6H8O6)稀溶液作底液;
②滴入足量Na2HPO4与CH3COONa混合溶液至pH=4;
③滴入含15.2g克FeSO4的溶液,最终维持pH=6,充分反应后静置;
④进行过滤和操作b,低温烘干得到磷酸亚铁晶体12.8克.
请回答下列问题:
(1)仪器A的名称是三颈烧瓶;
(2)配制FeSO4溶液时所用的蒸馏水应先进行的操作是煮沸除去水中的溶解的氧气.
(3)步骤④操作b的名称是洗涤,检验操作b是否完全的方法是取最后一次洗涤滤出液1-2mL于试管,滴入BaCl2溶液,若无白色沉淀,说明洗涤干净.
(4)抗坏血酸溶液的作用是防止磷酸亚铁被氧化.
(5)本实验的产率是76.5%(M[Fe3(PO4)2•8H2O]=502g•mol-1).
Ⅱ.水果和蔬菜中含有丰富的Vc,某研究性学习小组对它探究如下:
探究一:测定果汁中Vc的含量
分别向盛有lmL等浓度高锰酸钾稀溶液的四只试管中逐滴滴加梨汁、橙汁、苹果汁和0.04%的Vc溶液,边滴边振荡,直至高锰酸钾溶液褪色,测得以下数据:
(6)分析数据可知,三种果汁中Vc含量最高的是橙汁,其含量为0.02%;(各液体密度上的差别和每一滴的体积差别忽略不计).
探究二:蔬菜放置时间的长短对其Vc含量是否有影响
(7)请你用新鲜的西红柿、放置一周的西红柿、高锰酸钾稀溶液和必要的仪器设计实验方案:将新鲜西红柿和放置一周的西红柿分别捣碎,用纱布将汁液分别挤入两个烧杯中,向取有等量高锰酸钾稀溶液的两支试管中,分别滴入上述两种西红柿汁,边滴边振荡,直到高锰酸钾溶液刚好褪色,记录滴数..
 已知:①抗坏血酸(C6H8O6)(Vc)溶于水和乙醇,具有抗氧化性,可使酸性高锰酸钾溶液褪色;
已知:①抗坏血酸(C6H8O6)(Vc)溶于水和乙醇,具有抗氧化性,可使酸性高锰酸钾溶液褪色;②磷酸亚铁[Fe3(PO4)2•8H2O]为白蓝色单斜晶体,溶于稀酸,不溶于水、乙醇、醋酸.
I.磷酸亚铁是生产LiFePO4电池的原料,实验室利用FeSO4•7H2O、Na2HPO4•12H2O及CH3COONa•3H2O为原料制备磷酸亚铁晶体,合成时的主要反应为:
3FeSO4+2Na2HPO4+2CH3COONa+8H2O=Fe3(PO4)2•8H2O↓+3Na2SO4+2CH3COOH
装置如图所示:
实验步骤:
①在50mL干净的仪器A中加入抗坏血酸(C6H8O6)稀溶液作底液;
②滴入足量Na2HPO4与CH3COONa混合溶液至pH=4;
③滴入含15.2g克FeSO4的溶液,最终维持pH=6,充分反应后静置;
④进行过滤和操作b,低温烘干得到磷酸亚铁晶体12.8克.
请回答下列问题:
(1)仪器A的名称是三颈烧瓶;
(2)配制FeSO4溶液时所用的蒸馏水应先进行的操作是煮沸除去水中的溶解的氧气.
(3)步骤④操作b的名称是洗涤,检验操作b是否完全的方法是取最后一次洗涤滤出液1-2mL于试管,滴入BaCl2溶液,若无白色沉淀,说明洗涤干净.
(4)抗坏血酸溶液的作用是防止磷酸亚铁被氧化.
(5)本实验的产率是76.5%(M[Fe3(PO4)2•8H2O]=502g•mol-1).
Ⅱ.水果和蔬菜中含有丰富的Vc,某研究性学习小组对它探究如下:
探究一:测定果汁中Vc的含量
分别向盛有lmL等浓度高锰酸钾稀溶液的四只试管中逐滴滴加梨汁、橙汁、苹果汁和0.04%的Vc溶液,边滴边振荡,直至高锰酸钾溶液褪色,测得以下数据:
| 梨汁 | 苹果汁 | 橙汁 | 0.04%的Vc溶液 | |
| 滴加的滴数 | 40 | 20 | 10 | 5 |
探究二:蔬菜放置时间的长短对其Vc含量是否有影响
(7)请你用新鲜的西红柿、放置一周的西红柿、高锰酸钾稀溶液和必要的仪器设计实验方案:将新鲜西红柿和放置一周的西红柿分别捣碎,用纱布将汁液分别挤入两个烧杯中,向取有等量高锰酸钾稀溶液的两支试管中,分别滴入上述两种西红柿汁,边滴边振荡,直到高锰酸钾溶液刚好褪色,记录滴数..
17.反应A(g)+3B(g)?2C(g)+2D(g)在四种不同情况下的反应速率如下,其中表示反应速率最快的是( )
| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.015 mol/(L•s) | ||
| C. | v(C)=0.40 mol/(L•min) | D. | v(D)=0.45 mol/(L•min) |
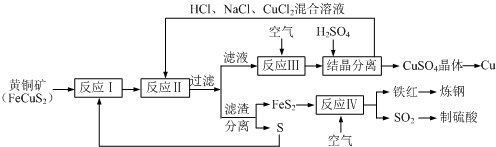
 )和抗癫痫药物H(
)和抗癫痫药物H(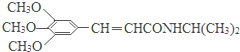 )的路线如图(部分反应略去条件和试剂):
)的路线如图(部分反应略去条件和试剂):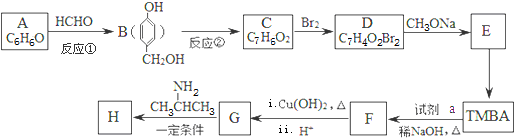
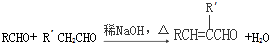 (R、R′表示烃基或氢)
(R、R′表示烃基或氢)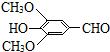 ,试剂a的分子式是C2H4O.
,试剂a的分子式是C2H4O. +2Br2→
+2Br2→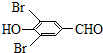 +2HBr.
+2HBr.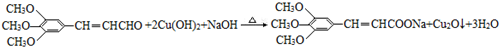 .
.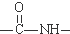 )有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式
)有类似酯基水解的性质,写出抗癫痫病药物H与足量NaOH溶液发生反应的化学方程式 +NaOH→
+NaOH→ +H2NCH(CH3)2.
+H2NCH(CH3)2.