题目内容
14.a、b、c、d为原子序数依次增大的短周期主族元素,a原子核外电子总数与b原子次外层的电子数相同;c所在周期数与族数相同;d与a同族,下列叙述正确的是( )| A. | 原子半径:d>c>b>a | B. | 4种元素中b的金属性最强 | ||
| C. | c的氧化物的水化物是强碱 | D. | d单质的氧化性比a单质的氧化性强 |
分析 a、b、c、d为原子序数依次增大的短周期主族元素,a原子核外电子总数与b原子次外层的电子数相同,则a的核外电子总数应为8,为O元素,则b、c、d为第三周期元素,c所在周期数与族数相同,应为Al元素,d与a同族,应为S元素,b可能为Na或Mg,结合对应单质、化合物的性质以及元素周期律解答该题.
解答 解:由以上分析可知a为O元素、b可能为Na或Mg、c为Al、d为S元素.
A.同周期元素从左到右原子半径逐渐减小,应为b>c>d,a为O,原子半径最小,故A错误;
B.同周期元素从左到右元素的金属性逐渐降低,则金属性b>c,a、d为非金属,金属性较弱,则4种元素中b的金属性最强,故B正确;
C.c为Al,对应的氧化物的水化物为氢氧化铝,为弱碱,故C错误;
D.一般来说,元素的非金属性越强,对应的单质的氧化性越强,应为a的单质的氧化性强,故D错误.
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,侧重考查学生的分析能力,本题注意把握原子核外电子排布的特点,把握性质的比较角度,难度不大.

练习册系列答案
相关题目
4.化学与生产、生活密切相关,下列叙述错误的是( )
| A. | 天然纤维和合成纤维的主要成分都是纤维素 | |
| B. | 海水淡化的方法有蒸馏法、离子交换法和电渗析法等 | |
| C. | 用乙醚从黄花蒿中提取青蒿素利用了萃取原理 | |
| D. | 水泥厂常用高压电除去工厂烟尘,利用了胶体的性质 |
5.合成药物异搏定路线中某一步骤如图所示,下列说法错误的是( )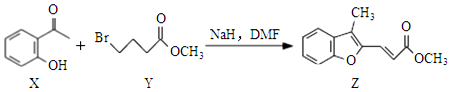
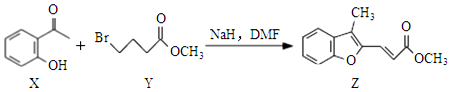
| A. | 物质X的分子中存在2种含氧官能团 | |
| B. | 物质Y可以发生水解和消去反应 | |
| C. | 1molZ最多可与2molBr2发生加成反应 | |
| D. | 等物质的量的X、Y分别与NaOH溶液反应,最多消耗的NaOH的物质的量之比为1:1 |
2.下列实验操作与预期实验目的或结论一致的是( )
| 实验操作 | 实验目的或结论 | |
| A | 某钾盐溶于盐酸.产生能使澄清石灰水变浑浊的无色无味气体 | 说明该钾盐是K2CO3 |
| B | 将FeCl2溶液加热蒸发 | 制备FeCl2晶体 |
| C | 向蔗糖溶液中加入稀硫酸,水浴加热后,加入新制氢氧化铜,加热,得到蓝色溶液 | 蔗糖水解的产物没有还原性 |
| D | 向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时间后过滤 | 除去MgCl2溶液中的少量FeCl3 |
| A. | A | B. | B | C. | C | D. | D |
9.下列指定反应的离子方程式正确的是( )
| A. | Cl2通入水中:Cl2+H2O?2H++Cl-+ClO- | |
| B. | 将铜丝插入浓硝酸中:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O | |
| C. | 将过氧化钠投入足量水中:2Na2O2+2H2O═4Na++4OH-+O2↑ | |
| D. | (NH4)2Fe(SO4)2溶液与过量Ba(OH)2溶液混合:Fe2++2SO42-+2Ba2++2OH-═Fe(OH)2↓+2BaSO4↓ |
19.下列说法正确的是( )
| A. | 植物油氢化过程中发生了加成反应 | |
| B. | 淀粉和纤维素互为同分异构体 | |
| C. | 环己烷与苯可用酸性KMnO4溶液鉴别 | |
| D. | 水可以用来分离溴苯和苯的混合物 |
2.古丝绸之路贸易中的下列商品,主要成分属于无机物的是( )
| A. |  瓷器 | B. |  丝绸 | C. |  茶叶 茶叶 | D. |  中草药 中草药 |
17.用沉淀滴定法快速测定NaI等碘化物溶液中c(I-),实验过程包括准备标准溶液和滴定待测溶液.
Ⅰ准备标准溶液
a.准确称取AgNO3基准物4.2468g(0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保存,备用.
b.配制并标定100mL 0.1000mol•L-1 NH4SCN标准溶液,备用.
Ⅱ滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中.
b.加入25.00mL 0.1000mol•L-1 AgNO3溶液(过量),使I-完全转化为AgI沉淀.
c.加入NH4Fe(SO4)2溶液作指示剂.
d.用0.1000mol•L-1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定.
e.重复上述操作两次.三次测定数据如下表:
f.数据处理.
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有250mL(棕色)容量瓶、胶头滴管.
(2)AgNO3标准溶液放在棕色试剂瓶中避光保存的原因是避免AgNO3见光分解.
(3)滴定应在pH<0.5的条件下进行,其原因是防止因Fe3+的水解而影响滴定终点的判断(或抑制Fe3+的水解).
(4)b和c两步操作是否可以颠倒否(或不能),说明理由若颠倒,Fe3+与I-反应,指示剂耗尽,无法判断滴定终点.
(5)所消耗的NH4SCN标准溶液平均体积为10.00mL,测得c(I-)=0.0600mol•L-1.
(6)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为用NH4SCN标准溶液进行润洗;.
(7)判断下列操作对c(I-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果偏高.
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果偏高.
Ⅰ准备标准溶液
a.准确称取AgNO3基准物4.2468g(0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保存,备用.
b.配制并标定100mL 0.1000mol•L-1 NH4SCN标准溶液,备用.
Ⅱ滴定的主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中.
b.加入25.00mL 0.1000mol•L-1 AgNO3溶液(过量),使I-完全转化为AgI沉淀.
c.加入NH4Fe(SO4)2溶液作指示剂.
d.用0.1000mol•L-1NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定.
e.重复上述操作两次.三次测定数据如下表:
| 实验序号 | 1 | 2 | 3 |
| 消耗NH4SCN标准溶液体积/mL | 10.24 | 10.02 | 9.98 |
回答下列问题:
(1)将称得的AgNO3配制成标准溶液,所使用的仪器除烧杯和玻璃棒外还有250mL(棕色)容量瓶、胶头滴管.
(2)AgNO3标准溶液放在棕色试剂瓶中避光保存的原因是避免AgNO3见光分解.
(3)滴定应在pH<0.5的条件下进行,其原因是防止因Fe3+的水解而影响滴定终点的判断(或抑制Fe3+的水解).
(4)b和c两步操作是否可以颠倒否(或不能),说明理由若颠倒,Fe3+与I-反应,指示剂耗尽,无法判断滴定终点.
(5)所消耗的NH4SCN标准溶液平均体积为10.00mL,测得c(I-)=0.0600mol•L-1.
(6)在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为用NH4SCN标准溶液进行润洗;.
(7)判断下列操作对c(I-)测定结果的影响(填“偏高”、“偏低”或“无影响”)
①若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,则测定结果偏高.
②若在滴定终点读取滴定管刻度时,俯视标准液液面,则测定结果偏高.
 某实验小组设计如下流程,模拟将汽车尾气中的氮氧化物(主要为NO和NO2的混合物)转化为工业用盐亚硝酸钠(NaNO2),并对亚硝酸钠进行多角度探究:汽车尾气$→_{操作①}^{20%NaOH}$溶液$\stackrel{操作②}{→}$固体$→_{③}^{操作}$NaNO2
某实验小组设计如下流程,模拟将汽车尾气中的氮氧化物(主要为NO和NO2的混合物)转化为工业用盐亚硝酸钠(NaNO2),并对亚硝酸钠进行多角度探究:汽车尾气$→_{操作①}^{20%NaOH}$溶液$\stackrel{操作②}{→}$固体$→_{③}^{操作}$NaNO2