题目内容
实验室用简易装置进行铝与氧化铁反应的实验中,发现生成的铁呈疏松多孔的褐色硬块,根据反应分析,褐色硬块除含有铁外,还可能含有氧化铝及未反应的氧化铁和铝等成分.
①先将褐色硬块处理成粉末,取少许粉末,加入一种试剂,根据实验现象排除铝的存在;
②另取一份粉末,按如下的流程进行实验;

(1)实验①中,选用的试剂是 ,证明不含铝的实验现象是 ;
(2)实验②中,多次进行过滤的分离方法,该实验中需要用到的玻璃仪器有 ,反应Ⅰ的离子方程式为 .滤液D的溶质的化学式为 ;
(3)通过上述实验,该同学认为褐色硬块除含铁外,还一定含有氧化铝,不含氧化铁,你认为该结论是伐可靠,并说明理由: .
①先将褐色硬块处理成粉末,取少许粉末,加入一种试剂,根据实验现象排除铝的存在;
②另取一份粉末,按如下的流程进行实验;

(1)实验①中,选用的试剂是
(2)实验②中,多次进行过滤的分离方法,该实验中需要用到的玻璃仪器有
(3)通过上述实验,该同学认为褐色硬块除含铁外,还一定含有氧化铝,不含氧化铁,你认为该结论是伐可靠,并说明理由:
考点:探究物质的组成或测量物质的含量,铁的氧化物和氢氧化物
专题:几种重要的金属及其化合物
分析:(1)金属铝可以和氢氧化钠发生反应产生氢气,所以可以取少量粉末加入NaOH溶液中,如果产生气泡证明含单质铝,反之则不含;
(2)依据过滤操作选择仪器;反应Ⅰ是铝、氧化铝和氢氧化钠溶液反应;过滤得到D中沉淀位氢氧化铝;
(3)原样品中的铁可能和溶解生成的铁离子发生反应生成亚铁离子;
(2)依据过滤操作选择仪器;反应Ⅰ是铝、氧化铝和氢氧化钠溶液反应;过滤得到D中沉淀位氢氧化铝;
(3)原样品中的铁可能和溶解生成的铁离子发生反应生成亚铁离子;
解答:
解:(1)金属铝可以和氢氧化钠发生反应产生氢气,所以可以取少量粉末加入NaOH溶液中,如果产生气泡证明含单质铝,反之则不含,
故答案为:氢氧化钠溶液;取少量粉末加入NaOH溶液中;无气泡冒出;
(2)实验②中,多次进行过滤的分离方法,该实验中需要用到的玻璃仪器有漏斗、玻璃棒、烧杯;反应Ⅰ是铝、氧化铝和氢氧化钠溶液反应,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,Al2O3+2OH-=H2O+2AlO2-;二氧化碳是过量,和偏铝酸钠溶液反应生成氢氧化铝沉淀和碳酸氢钠,滤液D的溶质的化学式为NaHCO3;
故答案为:漏斗、玻璃棒、烧杯,2Al+2OH-+2H2O=2AlO2-+3H2↑,Al2O3+2OH-=H2O+2AlO2-;NaHCO3;
(3)上述分析判断可知褐色硬块除含铁外,还一定含有氧化铝,氧化铁不能确定,因为原样品中的铁可能和溶解生成的铁离子发生反应生成亚铁离子,加入KSCN溶液后不变红色;
故答案为:不可靠,含有的铁可能把溶解生成的铁离子全部还原为亚铁离子,滴入KSCN溶液不变红色.
故答案为:氢氧化钠溶液;取少量粉末加入NaOH溶液中;无气泡冒出;
(2)实验②中,多次进行过滤的分离方法,该实验中需要用到的玻璃仪器有漏斗、玻璃棒、烧杯;反应Ⅰ是铝、氧化铝和氢氧化钠溶液反应,反应的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,Al2O3+2OH-=H2O+2AlO2-;二氧化碳是过量,和偏铝酸钠溶液反应生成氢氧化铝沉淀和碳酸氢钠,滤液D的溶质的化学式为NaHCO3;
故答案为:漏斗、玻璃棒、烧杯,2Al+2OH-+2H2O=2AlO2-+3H2↑,Al2O3+2OH-=H2O+2AlO2-;NaHCO3;
(3)上述分析判断可知褐色硬块除含铁外,还一定含有氧化铝,氧化铁不能确定,因为原样品中的铁可能和溶解生成的铁离子发生反应生成亚铁离子,加入KSCN溶液后不变红色;
故答案为:不可靠,含有的铁可能把溶解生成的铁离子全部还原为亚铁离子,滴入KSCN溶液不变红色.
点评:本题考查了物质组成的实验探究发现判断,物质性质的理解应用,离子检验的分析应用,掌握基础是关键,题目难度中等.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
X、Y、Z、R、W是原子序数依次增大的五种短周期元素.Y和R同主族,可组成共价化合物RY2,Y和Z最外层电子数之和与W的最外层电子数相同.25℃时,0.1mol/LX和W形成化合物的水溶液pH=1.下列说法正确的是( )
| A、Z与Y、Z与W形成的化合物的化学键完全相同 |
| B、Y、Z、W三种元素组成的化合物的水溶液可能显碱性 |
| C、简单离子的半径:Z>R>W>Y |
| D、因非金属Y>R,所以X与Y组成化合物的沸点低于X与R组成的化合物 |
除第1周期外,关于同周期主族元素的下列变化规律中正确的是( )
| A、从左到右,原子半径逐渐增大 |
| B、从左到右,元素原子氧化性减弱,还原性增强 |
| C、从左到右,元素最高正价从+1递增到+7(O,P除外),负价由-4递变到-1 |
| D、从左到右,元素最高价氧化物对应的水化物的碱性增强,酸性减弱(O,F除外) |
下列有关电化学装置的叙述正确的是( )
A、 Zn、MnO2干电池放电时MnO2被氧化 Zn、MnO2干电池放电时MnO2被氧化 |
B、 电解精炼铜时,阳极减少的质量与阴极增加的质量一定相等 电解精炼铜时,阳极减少的质量与阴极增加的质量一定相等 |
C、 K分别于M、N连接,均可保护Fe电极,且都称为“牺牲阳极的阴极保护法” K分别于M、N连接,均可保护Fe电极,且都称为“牺牲阳极的阴极保护法” |
D、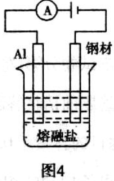 在钢材上电镀铝,熔融盐中Al和Cl元素只以AlCl4-、Al2Cl3-,形式存在,则阳极反应式为:Al-3e-+7AlCl4-=4Al2Cl3- 在钢材上电镀铝,熔融盐中Al和Cl元素只以AlCl4-、Al2Cl3-,形式存在,则阳极反应式为:Al-3e-+7AlCl4-=4Al2Cl3- |
空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池,如图为RFC工作原理示意图,有关说法,正确的是( )

| A、当有01mol电子转移时,a极产生1.21LO2(标准状况下) |
| B、b极上发生的电极反应是:4H2O+4e-=2H2↑+4OH- |
| C、c极发生的电极反应是:O2+2H2O+4e-=4OH- |
| D、d极上进行氧化反应,B中的H+可以通过隔膜进入A |
下列关于甲烷的说法正确的是( )
| A、属于高分子化合物 |
| B、与乙烷互为同分异构体 |
| C、不能发生氧化反应 |
| D、可用作燃料 |
 和
和 ; ⑥
; ⑥ 和
和 ⑦CH3(CH2)3CH3和
⑦CH3(CH2)3CH3和