题目内容
下列各组物质:
①O2和O3; ②1H、2H、3H; ③CH4和C10H22; ④乙烷和(CH3)2CHCH2CH3;
⑤ 和
和 ; ⑥
; ⑥ 和
和 ⑦CH3(CH2)3CH3和
⑦CH3(CH2)3CH3和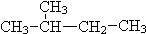
(1)互为同位素的是 ;
(2)互为同素异形体的是 ;
(3)互为同系物的是 ;
(4)互为同分异构体的是 ;
(5)属于同一物质的是 .(用序号填空)
①O2和O3; ②1H、2H、3H; ③CH4和C10H22; ④乙烷和(CH3)2CHCH2CH3;
⑤
 和
和 ; ⑥
; ⑥ 和
和 ⑦CH3(CH2)3CH3和
⑦CH3(CH2)3CH3和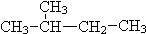
(1)互为同位素的是
(2)互为同素异形体的是
(3)互为同系物的是
(4)互为同分异构体的是
(5)属于同一物质的是
考点:同位素及其应用,同素异形体,同分异构现象和同分异构体
专题:
分析:根据同位素是指同一元素的不同原子;同素异形体是指同一元素的不同单质;同系物是指结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称同系物;同分异构体是指分子式相同结构不同的物质互称同分异构体;同一物质是指完全相同的物质来判断.
解答:
解:①O2和O3都是由氧元素组成的不同单质,则互为同素异形体;
②1H、2H、3H是质子数都是1,但中子数不同的原子,则互为同位素;
③CH4和C10H22都符合结构相似,在分子组成上相差一个或若干个CH2原子团的化合物,则互为同系物;
④乙烷和(CH3)2CHCH2CH3都符合结构相似,在分子组成上相差一个或若干个CH2原子团的化合物,则互为同系物;
⑤和 和
和 是同一种物质;
是同一种物质;
⑥ 和
和 前者是二元醇,后者是烷烃,既不是同系物也不是同分异构体;
前者是二元醇,后者是烷烃,既不是同系物也不是同分异构体;
⑦CH3 (CH2)3 CH3和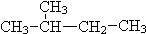 分子式相同,结构不同,属于同分异构体,故答案为:(1)②;(2)①;(3)③④;(4)⑦;(5)⑤.
分子式相同,结构不同,属于同分异构体,故答案为:(1)②;(2)①;(3)③④;(4)⑦;(5)⑤.
②1H、2H、3H是质子数都是1,但中子数不同的原子,则互为同位素;
③CH4和C10H22都符合结构相似,在分子组成上相差一个或若干个CH2原子团的化合物,则互为同系物;
④乙烷和(CH3)2CHCH2CH3都符合结构相似,在分子组成上相差一个或若干个CH2原子团的化合物,则互为同系物;
⑤和
 和
和 是同一种物质;
是同一种物质;⑥
 和
和 前者是二元醇,后者是烷烃,既不是同系物也不是同分异构体;
前者是二元醇,后者是烷烃,既不是同系物也不是同分异构体;⑦CH3 (CH2)3 CH3和
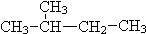 分子式相同,结构不同,属于同分异构体,故答案为:(1)②;(2)①;(3)③④;(4)⑦;(5)⑤.
分子式相同,结构不同,属于同分异构体,故答案为:(1)②;(2)①;(3)③④;(4)⑦;(5)⑤.
点评:本题主要考查的是同系物、同分异构体、同位素的概念等,难度不大,属于常考题.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
X、Y、Z均为短周期元素,其中X、Z处于同一主族,且Z的原子序数是X的原子序数的两倍;X、Y的最简单离子具有相同的电荷数,但电性相反,且具有相同的电子层结构.下列说法正确的是( )
| A、Y、Z处于同一周期 |
| B、X的最高价是+6价 |
| C、原子半径:Z>Y>X |
| D、非金属性:X>Y>Z |
已知:Fe2O3(s)+
C(s)=
CO2(g)+2Fe(s)△H=234.1kJ?mol-1 C(s)+O2(g)=CO2(g)△H=-393.5kJ?mol-1则2Fe(s)+
O2(g )=Fe2O3(s) 的△H是( )
| 3 |
| 2 |
| 3 |
| 2 |
| 3 |
| 2 |
| A、-824.4kJ?mol-1 |
| B、-627.6kJ?mol-1 |
| C、-744.7kJ?mol-1 |
| D、-169.4kJ?mol-1 |
下列有机反应属于加成反应的是( )
A、C2H5OH+CH3COOH
| |||
B、H-C≡C-H+HCl
| |||
C、 | |||
D、 |
下列关于元素周期表的说法正确的是( )
| A、元素的性质随着原子的相对质量的递增而呈周期性变化的规律叫做元素周期律 |
| B、X2+的核外电子数目为18,则X在第三周期第ⅥA族 |
| C、因K比Na容易失去电子,所以金属性K比Na强 |
| D、Li、Na、K元素的原子随着核电荷数的增加核外电子层数减少 |

