题目内容
根据反应Br+H2?HBr+H的能量对反应历程的示意图甲进行判断,下列叙述中不正确的是( )
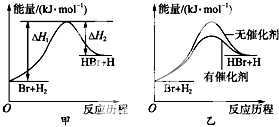

| A、正反应吸热 |
| B、加入催化剂,该化学反应的反应热不变 |
| C、加入催化剂后,该反应的能量对反应历程的示意图可用图乙表示 |
| D、加入催化剂可增大正反应速率,降低逆反应速率 |
考点:反应热和焓变,化学反应速率的影响因素
专题:化学反应中的能量变化
分析:根据反应物的总能量小于生成物的总能量,可知反应吸热,
A、正反应为吸热反应;
B、催化剂不影响反应物和生成物能量高低;
C、催化剂能够降低反应的活化能;
D、催化剂能够同等程度地增大正逆反应速率.
A、正反应为吸热反应;
B、催化剂不影响反应物和生成物能量高低;
C、催化剂能够降低反应的活化能;
D、催化剂能够同等程度地增大正逆反应速率.
解答:
解:根据反应物的总能量小于生成物的总能量,可知反应吸热,
A、因正反应为吸热反应,故A正确;
B、催化剂不影响反应物和生成物能量高低,不影响反应热,故B正确;
C、催化剂能够降低反应的活化能,加快反应速率,故C正确;
D、催化剂能够同等程度地增大正逆反应速率,故D错误;
故选D.
A、因正反应为吸热反应,故A正确;
B、催化剂不影响反应物和生成物能量高低,不影响反应热,故B正确;
C、催化剂能够降低反应的活化能,加快反应速率,故C正确;
D、催化剂能够同等程度地增大正逆反应速率,故D错误;
故选D.
点评:本题考查了催化剂对反应速率的影响原因以及据图分析反应热的大小,题目难度不大.

练习册系列答案
相关题目
实验中需用2.0mol?L-1的Na2CO3溶液950mL,配制时应选用容量瓶的规格和称取Na2CO3固体的质量分别为( )
| A、950 mL;201.4 g |
| B、1 000 mL;212.0 g |
| C、100 mL;21.2 g |
| D、500 mL;100.7 g |
某金属能与盐酸反应产生氢气,该金属与锌组成的原电池中,锌为负极.该金属为( )
| A、铝 | B、铜 | C、铁 | D、镁 |
热化学方程式C(s)+H2O(g)═CO(g)+H2(g)△H=+131.3kJ?mol-1表示…( )
| A、碳和水反应吸收131.3 kJ能量 |
| B、1个固态碳原子和1分子水蒸气反应吸热131.3 kJ |
| C、1 mol碳和1 mol水反应生成1 mol一氧化碳和1 mol氢气并吸收131.3 kJ热量 |
| D、1 mol固态碳和1 mol水蒸气反应生成1 mol一氧化碳气体和1 mol氢气并吸收131.3 kJ热量 |
已知1gH2完全燃烧生成水蒸气放出热量为121KJ,并且H-H键能为436KJ/mol,1molO=O键完全断裂时吸收的热量为496KJ,则形成1molH-O键放出的热量为( )
| A、436KJ |
| B、463KJ |
| C、649KJ |
| D、869KJ |
N2、O2、CO2按体积比为1:2:3组成的混合气体共50g,在标准状况下的体积为( )
| A、60L | B、30L |
| C、11.2L | D、112L |
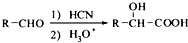 ,写出由C制备化合物
,写出由C制备化合物 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:CH3CH2OH