题目内容
某金属能与盐酸反应产生氢气,该金属与锌组成的原电池中,锌为负极.该金属为( )
| A、铝 | B、铜 | C、铁 | D、镁 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:根据金属的活泼性来判断两种金属与酸构成的原电池中的负极,活泼金属作负极.
解答:
解:因金属活泼性为Mg>Al>Fe>Cu,
该金属与锌组成原电池时,锌为负极,
则该金属为Fe或Cu,但Cu与盐酸不反应,只有Fe符合,
故选C.
该金属与锌组成原电池时,锌为负极,
则该金属为Fe或Cu,但Cu与盐酸不反应,只有Fe符合,
故选C.
点评:本题考查原电池,为高频考点,侧重于学生的分析能力的考查,熟悉金属的活泼性是解答本题的关键,注意金属为盐酸反应的特点,为易错点,题目较简单.

练习册系列答案
相关题目
你不慎将一杯水倒入家中的菜油中,最好采用下列何种方法分离( )
| A、过滤 | B、分液 | C、蒸馏 | D、萃取 |
根据反应Br+H2?HBr+H的能量对反应历程的示意图甲进行判断,下列叙述中不正确的是( )
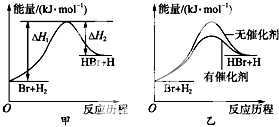

| A、正反应吸热 |
| B、加入催化剂,该化学反应的反应热不变 |
| C、加入催化剂后,该反应的能量对反应历程的示意图可用图乙表示 |
| D、加入催化剂可增大正反应速率,降低逆反应速率 |
三聚氰胺的结构简式如图,下列说法不正确的是( )
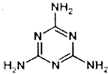

| A、三聚氰胺分子式C3N6H6,相对分子质量126 |
| B、已知合成三聚氰胺的反应是:6(NH2)CO→C3N6H6+6NH3+3CO2,反应物是尿素 |
| C、三聚氰胺分子所有原子在一个平面上 |
| D、三聚氰胺呈弱碱性,与盐酸、硫酸、硝酸、乙酸、草酸等都能形成三聚氰胺盐 |
下列叙述正确的是( )
| A、同温同压下,相同体积的气体,其分子数一定相等,原子数也一定相等 |
| B、任何条件下,等物质的量的甲烷(CH4)和一氧化碳所含的原子数一定相等 |
| C、同温同压下的一氧化碳气体和氮气,若体积相等,则质量一定相等 |
| D、1L一氧化碳气体一定比1L氧气的质量小 |