题目内容
在反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2+8H2O中,氧化产物与还原产物物质的量之比是 ,若有7.3g HCl被氧化,转移的电子数为 mol.
考点:氧化还原反应
专题:氧化还原反应专题
分析:氧化还原反应中,化合价升高的元素被氧化,对应产物是氧化产物,化合价降低元素被还原,所在的反应物是氧化剂,发生还原反应,对应产物是还原产物;根据化学方程式和转移的电子数目来计算氯气和转移电子的量的情况.
解答:
解:氧化还原反应2KMnO4+16HCl(浓)═2KCl+2MnCl2+5Cl2↑+8H2O中,化合价升高的Cl元素被氧化,对应产物Cl2是氧化产物,化合价降低的Mn元素被还原,所在的反应物KMnO4是氧化剂,发生还原反应,对应产物MnCl2是还原产物,氧化产物与还原产物的物质的量之比为5:2;
若有7.3g即0.2molHCl被氧化,转移电子的物质的量为0.2mol,
故答案为:5:2;0.2.
若有7.3g即0.2molHCl被氧化,转移电子的物质的量为0.2mol,
故答案为:5:2;0.2.
点评:本题考查学生氧化还原反应的基本概念和电子转移知识,注意把握氧化剂、还原剂、氧化产物、还原产物等概念,题目难度不大.

练习册系列答案
相关题目
在NaIO3的碱性溶液中通入Cl2,可用得到Na2H3IO6.对于该反应的说法正确的是( )
| A、每生成1mol Na2H3IO6转移2mol电子 |
| B、碱性条件下,NaIO3的氧化性强于Na2H3IO6 |
| C、该反应中Cl2做还原剂 |
| D、氧化产物与还原产物的物质的量之比为2:1 |
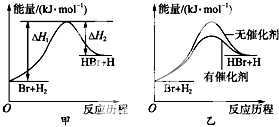
根据反应Br+H2?HBr+H的能量对反应历程的示意图甲进行判断,下列叙述中不正确的是( )

| A、正反应吸热 |
| B、加入催化剂,该化学反应的反应热不变 |
| C、加入催化剂后,该反应的能量对反应历程的示意图可用图乙表示 |
| D、加入催化剂可增大正反应速率,降低逆反应速率 |
某饮用水的理化指标:钙≥4.0mg/L、钾≥0.35mg/L、钠≥0.8mg/L、镁≥0.5mg/L,以上钙、钾、钠、镁指的是( )
| A、分子 | B、氧化物 | C、元素 | D、单质 |
三聚氰胺的结构简式如图,下列说法不正确的是( )
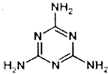

| A、三聚氰胺分子式C3N6H6,相对分子质量126 |
| B、已知合成三聚氰胺的反应是:6(NH2)CO→C3N6H6+6NH3+3CO2,反应物是尿素 |
| C、三聚氰胺分子所有原子在一个平面上 |
| D、三聚氰胺呈弱碱性,与盐酸、硫酸、硝酸、乙酸、草酸等都能形成三聚氰胺盐 |
某气体通入品红溶液,溶液褪色,加热后恢复红色,则该气体是( )
| A、N2 |
| B、SO2 |
| C、O2 |
| D、H2 |