题目内容
某一反应体系中涉及的反应物和生成物共有4种物质:X、Cl2、NH3、N2.当转移的电子总数为a个时,氮气数量变化了bmol.
(1)氧化产物的摩尔质量是
(2)阿伏加德罗数常数为(用含a、b的代数式表示) .
(3)X可能有两种组成:HCl、NH4Cl,为确定X的化学式,某同学分别取同温同压下体积分别为V1、V2的两种物质(氧化剂与还原剂)充入一恒压、容积可变的密闭容器中,在一定条件下反应完全并恢复到原温后,再测出容器的容积(V3).
①若实验结果(用V1、V2与V3间关系来表示,后同)是 ,则X的化学式一定为HCl.
②若实验结果是 ,则X的化学式为NH4Cl.
(1)氧化产物的摩尔质量是
(2)阿伏加德罗数常数为(用含a、b的代数式表示)
(3)X可能有两种组成:HCl、NH4Cl,为确定X的化学式,某同学分别取同温同压下体积分别为V1、V2的两种物质(氧化剂与还原剂)充入一恒压、容积可变的密闭容器中,在一定条件下反应完全并恢复到原温后,再测出容器的容积(V3).
①若实验结果(用V1、V2与V3间关系来表示,后同)是
②若实验结果是
考点:阿伏加德罗定律及推论
专题:阿伏加德罗常数和阿伏加德罗定律
分析:(1)氯气具有强氧化性,所以作氧化剂,化合价由0价变为-1价,则氨气作还原剂,化合价升高,所以氧化产物是氮气;
(2)生成1molN2时转移6mol电子,故有NA:6=a:b,据此计算阿伏伽德罗常数;
(3)当X为HCl时,NH3肯定反应完了,由方程式2NH3+3Cl2=N2+6HCl结合阿伏伽德罗定律解答;
当V为NH4Cl,Cl2肯定反应完了,由8NH3+3Cl2=N2+6NH4Cl及阿伏伽德罗定律解答.
(2)生成1molN2时转移6mol电子,故有NA:6=a:b,据此计算阿伏伽德罗常数;
(3)当X为HCl时,NH3肯定反应完了,由方程式2NH3+3Cl2=N2+6HCl结合阿伏伽德罗定律解答;
当V为NH4Cl,Cl2肯定反应完了,由8NH3+3Cl2=N2+6NH4Cl及阿伏伽德罗定律解答.
解答:
解:(1)从氮元素价态知对应反应为氧化还原反应,因Cl2有强氧化性,氨气中N元素化合价为-3价、氮气中N元素化合价为0价,故NH3是还原剂,N2是氧化产物28g?mol -1,故答案为:28g/mol;
(2)生成1molN2时转移6mol电子,故有1:6=
:b,NA=
mol-1,
故答案为:
mol-1;
(3)①当X为HCl时,NH3肯定反应完了,由方程式2NH3+3Cl2=N2+6HCl及阿伏加德罗定律可推出V3=2V2+V1,故答案为:V3=2V2+V1;
②当V为NH4Cl,Cl2肯定反应完了,由8NH3+3Cl2=N2+6NH4Cl阿伏加德罗定律可推出V3=V2-
V1,故答案为:V3=V2-
V1.
(2)生成1molN2时转移6mol电子,故有1:6=
| a |
| NA |
| 6a |
| b |
故答案为:
| 6a |
| b |
(3)①当X为HCl时,NH3肯定反应完了,由方程式2NH3+3Cl2=N2+6HCl及阿伏加德罗定律可推出V3=2V2+V1,故答案为:V3=2V2+V1;
②当V为NH4Cl,Cl2肯定反应完了,由8NH3+3Cl2=N2+6NH4Cl阿伏加德罗定律可推出V3=V2-
| 7 |
| 3 |
| 7 |
| 3 |
点评:本题考查阿伏伽德罗定律及氧化还原反应,明确常见物质的性质及阿伏伽德罗定律内涵是解本题关键,难点是阿伏伽德罗定律的灵活运用,题目难度中等.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质.其工作原理如图所示:下列关于固体燃料电池的有关说法正确的是( )
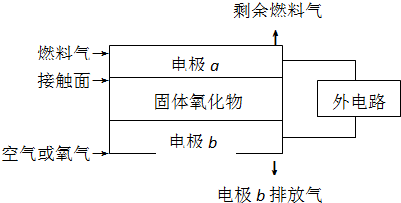

| A、电极b为电池负极,电极反应式为2O2+4e-=4O2- |
| B、固体氧化物的作用是让电子在电池内通过 |
| C、若H2作为燃料气,则接触面上发生的反应为H2+2OH--4e-=2H++H2O |
| D、若C2H4作为燃料气,则接触面上发生的反应为C2H4+6O2--12e-=2CO2+2H2O |
下列说法或表示方法正确的是( )
| A、等物质的量的硫蒸汽和硫固体分别完全燃烧,前者放出热量比后者少 |
| B、由C(石墨)=C(金刚石);△H=+1.90 kJ?mol-1可知,金刚石比石墨稳定 |
| C、在101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,则表示氢气燃烧热的热化学方程式为:2H2(g)+O2(g)═2H2O(l);△H=-571.6 kJ?mol-1 |
| D、在稀溶液中,H+(aq)+OH-(aq)═H2O(1);△H=一57.3 kJ?mol-1,若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ |
等物质的量的CH4和NH3相比较,下列结论错误的是?( )
| A、它们的分子个数比为1:1 |
| B、它们的原子个数比为5:4 |
| C、它们的电子个数比为1:1 |
| D、它们的体积比为1:1 |
下列说法中正确的是( )
| A、电解质的水溶液一定能导电 |
| B、非电解质的水溶液一定不能导电. |
| C、液态酒精、酒精的水溶液不导电,所以酒精是非电解质 |
| D、HCl的水溶液能导电,所以HCl是电解质 |
下列各组物质,前者属于电解质,后者属于非电解质的是( )
| A、NaCl晶体、BaSO4 |
| B、液态的醋酸、酒精 |
| C、铜、二氧化硫 |
| D、熔融的KNO3、硫酸溶液 |