题目内容
等物质的量的CH4和NH3相比较,下列结论错误的是?( )
| A、它们的分子个数比为1:1 |
| B、它们的原子个数比为5:4 |
| C、它们的电子个数比为1:1 |
| D、它们的体积比为1:1 |
考点:阿伏加德罗定律及推论
专题:
分析:A.由N=nNA可知,分子数目之比等于物质的量之比;
B.结合分子含有原子数目计算;
C.CH4、NH3分子都含有10个电子,物质的量相等,含有电子数目相等;
D.根据V=nVm计算体积.
B.结合分子含有原子数目计算;
C.CH4、NH3分子都含有10个电子,物质的量相等,含有电子数目相等;
D.根据V=nVm计算体积.
解答:
解:A.由N=nNA可知,等物质的量的CH4和NH3中分子数目之比等于物质的量之比为1:1,故A正确;
B.CH4、NH3分子含有原子数目分别为5、4,故等物质的量的CH4和NH3中含有H原子数目之比=5:4,故B正确;
C.CH4、NH3分子都含有10个电子,物质的量相等,含有电子总数为1:1,故C正确;
D.等物质的量的CH4和NH3,它们的体积比为nVm之比,但是Vm无法判断,所以体积之比无法确定,故D错误,
故选D.
B.CH4、NH3分子含有原子数目分别为5、4,故等物质的量的CH4和NH3中含有H原子数目之比=5:4,故B正确;
C.CH4、NH3分子都含有10个电子,物质的量相等,含有电子总数为1:1,故C正确;
D.等物质的量的CH4和NH3,它们的体积比为nVm之比,但是Vm无法判断,所以体积之比无法确定,故D错误,
故选D.
点评:本题考查物质的量有关计算、分子中含有微粒计算,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
科学家P?Tatapudi等人首先使用在空气中电解水(酸性)的方法,在阳极制得臭氧,阴极制得过氧化氢.电解总方程式为:3H2O+3O2?3H2O2+O3,下列说法正确的是( )
| A、阳极反应:3O2+6e-+6H+=3H2O2 |
| B、氧化性:O2>O3 |
| C、电解一段时间后,溶液pH下降 |
| D、每转移3 mol电子,可生成标准状况下22.4 L O3 |
下列事实,不能用勒沙特列原理解释的是( )
| A、溴水中有下列平衡Br2+H2O?HBr+HBrO 当加入AgNO3溶液后,溶液颜色变浅 |
| B、合成NH3反应,为提高NH3的产率,理论上应采取低温度的措施 |
| C、反应CO+NO2?CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动 |
| D、对2HI(g)?H2(g)+I2(g),平衡体系增大压强可使颜色变深 |
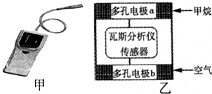 瓦斯爆炸是煤矿开采中的重大危害及事故发生源,一种瓦斯分析仪(图甲)的传感器在煤矿巷道中的甲烷达到一定浓度时会自动报警,大大减少了事故发生率.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y学科王2O3-Na2O,O2-可以在其中自由移动.则下列有关叙述不正确的是( )
瓦斯爆炸是煤矿开采中的重大危害及事故发生源,一种瓦斯分析仪(图甲)的传感器在煤矿巷道中的甲烷达到一定浓度时会自动报警,大大减少了事故发生率.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y学科王2O3-Na2O,O2-可以在其中自由移动.则下列有关叙述不正确的是( )| A、电极a的反应式为:CH4+4O2--8e-=CO2+2H2O |
| B、电极b是正极,O2-由电极b流向电极a |
| C、瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a |
| D、当固体电解质中有1 molO2-通过时,电子转移2 mol |
由如图分析,有关叙述正确的是( )
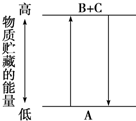

| A、A-→B+C和B+C-→A两个反应吸收或放出的能量不等 |
| B、A-→B+C是放热反应 |
| C、A具有的能量高于B和C具有的能量总和 |
| D、A-→B+C是吸热反应,则B+C-→A必然是放热反应 |
下列各组离子一定能大量共存的是( )
| A、在无色溶液中:NH4+、Fe2+、SO42-、CO32- |
| B、加铝粉产生氢气的溶液中:NH4+、NO3?、Cl?、Ba2+ |
| C、在pH=1的溶液中:K+、Fe2+、Cl-、CH3COO- |
| D、含有0.1 mol?L-1H2SO4的溶液中:K+、Mg2+、Cl-、NO3- |
用盐酸测定碳酸钠时既可用酚酞作指示剂又可用甲基橙(一种酸碱指示剂)作指示剂,现分别用酚酞和甲基橙作指示剂,用0.1000mol/L的HCl滴定20.00mL的纯碱溶液,滴定终点时分别用去了20.00mL、40.00mL的盐酸,下列说法中不正确的是( )
| A、用酚酞作指示剂时滴定的总反应为:Na2CO3+HCl═NaHCO3+NaCl |
| B、用甲基橙作指示剂时滴定的总反应为:Na2CO3+2HCl═NaCl+CO2↑+H2O |
| C、可用碱式滴定管量取所需要的Na2CO3溶液 |
| D、若酸式滴定管没有用标准溶液润洗,则所测得的碳酸钠溶液浓度偏低 |