题目内容
(1)6.02×1022个NH3分子的质量为 g,标准状况下的体积为 L,与 g CH4中含有的氢原子数相等.
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448ml,则该氧化物的摩尔质量为 ,R的相对原子质量为 .
(3)将20gNaOH固体溶于100ml水中配成溶液,所得溶液的密度为1.2g/ml,则该溶液的物质的量浓度为 .
(2)某气体氧化物的化学式为RO2,在标准状况下,1.28g该氧化物的体积为448ml,则该氧化物的摩尔质量为
(3)将20gNaOH固体溶于100ml水中配成溶液,所得溶液的密度为1.2g/ml,则该溶液的物质的量浓度为
考点:物质的量的相关计算
专题:计算题
分析:(1)根据n=
计算氨气物质的量,根据m=nM计算其质量,根据V=nVm计算氨气体积,计算甲烷的物质的量,根据m=nM计算甲烷的质量;
(2)根据n=
计算RO2的物质的量,再根据M=
计算其摩尔质量,进而计算R的相对原子质量;
(3)计算溶液中氢氧化钠的质量分数,再根据c=
计算氢氧化钠的物质的量浓度.
| m |
| M |
(2)根据n=
| V |
| Vm |
| m |
| n |
(3)计算溶液中氢氧化钠的质量分数,再根据c=
| 1000ρω |
| M |
解答:
解:(1)6.02×1022个NH3分子的物质的量为
=0.1mol,其质量为0.1mol×17g/mol=1.7g,标况下,氨气体积为0.1mol×22.4L/mol=2.24L,与之含有相等氢原子数目的甲烷为
=0.075mol,甲烷的质量为0.075mol×16g/mol=1.2g,
故答案为:1.7;2.24;1.2;
(2)RO2的物质的量的物质的量为
=0.02mol,其摩尔质量为
=64g/mol,R的相对原子质量为64-32=32,
故答案为:64g/mol;32;
(3)100ml水的质量为100g,溶液中氢氧化钠的质量分数为
=
,根据c=
可知,氢氧化钠的物质的量浓度为
mol/L=5mol/L,故答案为:5mol/L.
| 6.02×1022 |
| 6.02×1023mol-1 |
| 0.1mol×3 |
| 4 |
故答案为:1.7;2.24;1.2;
(2)RO2的物质的量的物质的量为
| 0.448L |
| 22.4L/mol |
| 1.28g |
| 0.02mol |
故答案为:64g/mol;32;
(3)100ml水的质量为100g,溶液中氢氧化钠的质量分数为
| 20g |
| 100g+20g |
| 1 |
| 6 |
| 1000ρω |
| M |
1000×1.2×
| ||
| 40 |
点评:本题考查物质的量有关计算,比较基础,注意掌握与物质的量为中心的有关计算.

练习册系列答案
 名校通行证有效作业系列答案
名校通行证有效作业系列答案
相关题目
下列关于离子晶体的描述不正确的是( )
| A、离子晶体是阳离子和阴离子通过静电吸引力结合而成的晶体 |
| B、晶格能由大到小:NaF>NaCl>NaBr>NaI |
| C、硬度:MgO>CaO>BaO |
| D、在氯化钠晶体中,Na+和Cl-的配位数均为6 |
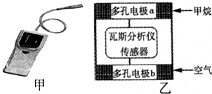 瓦斯爆炸是煤矿开采中的重大危害及事故发生源,一种瓦斯分析仪(图甲)的传感器在煤矿巷道中的甲烷达到一定浓度时会自动报警,大大减少了事故发生率.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y学科王2O3-Na2O,O2-可以在其中自由移动.则下列有关叙述不正确的是( )
瓦斯爆炸是煤矿开采中的重大危害及事故发生源,一种瓦斯分析仪(图甲)的传感器在煤矿巷道中的甲烷达到一定浓度时会自动报警,大大减少了事故发生率.该瓦斯分析仪工作原理类似燃料电池的工作原理,其装置如图乙所示,其中的固体电解质是Y学科王2O3-Na2O,O2-可以在其中自由移动.则下列有关叙述不正确的是( )| A、电极a的反应式为:CH4+4O2--8e-=CO2+2H2O |
| B、电极b是正极,O2-由电极b流向电极a |
| C、瓦斯分析仪工作时,电池内电路中电子由电极b流向电极a |
| D、当固体电解质中有1 molO2-通过时,电子转移2 mol |
下列各组离子一定能大量共存的是( )
| A、在无色溶液中:NH4+、Fe2+、SO42-、CO32- |
| B、加铝粉产生氢气的溶液中:NH4+、NO3?、Cl?、Ba2+ |
| C、在pH=1的溶液中:K+、Fe2+、Cl-、CH3COO- |
| D、含有0.1 mol?L-1H2SO4的溶液中:K+、Mg2+、Cl-、NO3- |
两份体积相同的某植物营养液,其配方如下:①②两份营养液的成分(所含离子)( )
| 成分 含量 编号 | KCl | K2SO4 | ZnSO4 | ZnCl2 |
| ① | 0.3mol | 0.2mol | 0.1mol | - |
| ② | 0.1mol | 0.3mol | - | 0.1mol |
| A、仅n(K+)相同 |
| B、仅n(Cl-)相同 |
| C、不完全相同 |
| D、完全相同 |
