题目内容
12.下列实验现象所对应的离子方程式不正确的是( )| 实验 | 现象 | 离子方程式 | |
| A |  | 在空气中放置一段时间后,溶液呈蓝色 | 4H++4I-+O2═2I2+2H2O |
| B | 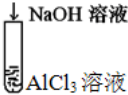 | 溶液由先浑浊后澄清 | Al3++3OH-═Al(OH)3↓ Al(OH)3+OH-═AlO2-+2H2O |
| C | 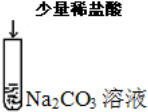 | 溶液中无气泡产生 | CO22-+H+=HCO3-+H2O |
| D |  | 有白色沉淀生成,溶液由红色变为无色 | Ba2++OH-+H++SO42-═BaSO4↓+H2O |
| A. | A | B. | B | C. | C | D. | D |
分析 A.I-具有较强的还原性,在酸性溶液中可被空气中的O2氧化成I2,I2遇淀粉溶液变为蓝色,该反应现象与对应的离子方程式一致,故A正确;
B.AI(OH)3有两性,可溶于强碱溶液生成AlO2-,加入碱少量时生成氢氧化铝沉淀,当碱过量时氢氧化铝溶解生成偏铝酸钠;
C.盐酸不足时,碳酸钠与盐酸反应生成碳酸氢钠,无CO2气体生成;
D.该离子方程式中得到氢离子、氢氧根离子的系数与硫酸、氢氧化钡的化学式不相符.
解答 解:A.I-具有较强的还原性,在酸性溶液中可被空气中的O2氧化成I2,I2遇淀粉溶液变为蓝色,反应的离子方程式为:4H++4I-+O2═2I2+2H2O,故A正确;
B.AI(OH)3有两性,可溶于强碱溶液生成AlO2-,所以加入碱少量时,发生反应:Al3++3OH-=Al(OH)3↓,当碱过量时又发生反应:Al(OH)3+OH-=AlO2-+2H2O,故B正确;
C.Na2CO3溶液和稀盐酸分步反应,盐酸不足时,发生反应:Na2CO3+HCl=NaCl+NaHCO3,生成NaHCO3,无CO2气体生成,故C正确;
D.氢离子、氢氧根离子的系数错误,H2SO4和Ba(OH)2反应的离子方程式应为:Ba2++2OH-+2H-+SO42-=BaSO4↓+2H2O,故D错误;
故选D.
点评 本题考查化学实验方案的设计与评价,涉及化学操作、实验现象及所对应的离子方程式正误判断等知识,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,试题培养了学生的灵活应用能力.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
20.下列说法正确的是( )
| A. | SiO2与所有的酸都不能发生反应 | |
| B. | 将CO2、SO2通入Ca(ClO)2溶液均发生反应且反应类型相同 | |
| C. | 过量的铜与浓硝酸反应能生成NO气体 | |
| D. | 加盐酸产生能使澄清石灰水变浑浊气体的钠盐为Na2CO3 |
17.历史上最早应用的还原性染料是靛蓝,其结构简式如图所示,下列关于靛蓝的叙述中错误的是( )
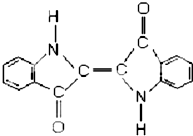

| A. | 靛蓝由碳、氢、氧、氮四种元素组成 | B. | 它的分子式是 C16H10N2O2 | ||
| C. | 该物质是苯的同系物 | D. | 它含有碳碳双键、羰基等官能团 |
1.下列说法正确的是( )
| A. | 分子式为C2H6O的有机化合物性质相同 | |
| B. | 相同条件下,等质量的碳按a、b两种途径完全转化,途径a比途径b放出更多热能 途径a:C$→_{高温}^{H_{2}O}$CO+H2$→_{燃烧}^{O_{2}}$CO2+H2O 途径b:C$→_{燃烧}^{O_{2}}$CO2 | |
| C. |  可以表示乙醇分子的球棍模型 可以表示乙醇分子的球棍模型 | |
| D. |  :既可以表示甲烷分子,也可以表示四氯化碳分子 :既可以表示甲烷分子,也可以表示四氯化碳分子 |
2.下列指定反应的离子方程式正确的是( )
| A. | [Ag(NH3)2]OH的溶液中加入盐酸:Ag++Cl-═AgCl↓ | |
| B. | NaAlO2溶液中通入过量的CO2:2AlO2-+3H2O+CO2═2Al(OH)3↓+CO32- | |
| C. | 用Na2S2O3溶液吸收自来水中多余Cl2:4Cl2+S2O32-+5H2O═10H++2SO42-+8Cl- | |
| D. | 向酸性KMnO4溶液滴加H2C2O4(弱酸),溶液褪色:2MnO4++5H2C2O4═2Mn2++10CO2↑+2H2O+6OH- |
 化学中的某些元素与生命活动密不可分.请回答下列问题:
化学中的某些元素与生命活动密不可分.请回答下列问题:
 ,元素c在周期表的位置第二周期IVA族
,元素c在周期表的位置第二周期IVA族