题目内容
17.已知不同条件下,磷与硫酸铜可以发生如下两个反应:①2P+5CuSO4+8H2O=5Cu+2H3PO4+5H2SO4
②11P+15CuSO4+24H2O=5Cu3P+6H3PO4+15H2SO4
下列叙述正确的是( )
| A. | 反应①中,氧化剂与还原剂的物质的量之比为2:5 | |
| B. | 反应②中,Cu3P既是氧化产物又是还原产物 | |
| C. | 反应②中,当有5mol CuSO4发生反应时,共转移电子10mol | |
| D. | 反应①中CuSO4做氧化剂,反应②中CuSO4作还原剂 |
分析 2P+5CuSO4+8H2O═5Cu+2H3PO4+5H2SO4该反应中P元素化合价由0价变为5价,Cu元素化合价由+2价变为0价;11P+15CuSO4+24H2O═5Cu3P+6H3PO4+15H2SO4该反应中P元素化合价由0价变为-3价、+5价,Cu元素化合价由+2价变为+1价,如果有11molP参加氧化还原反应,则有$\frac{6}{11}$的P被氧化,其余的P被还原,据此分析解答.
解答 解:2P+5CuSO4+8H2O═5Cu+2H3PO4+5H2SO4该反应中P元素化合价由0价变为5价,Cu元素化合价由+2价变为0价;
11P+15CuSO4+24H2O═5Cu3P+6H3PO4+15H2SO4该反应中P元素化合价由0价变为-3价、+5价,Cu元素化合价由+2价变为+1价,如果有11molP参加氧化还原反应,则有$\frac{6}{11}$的P被氧化,其余的P被还原,
A、反应①中,氧化剂与还原剂的物质的量之比为5:2,故A错误;
B、反应②中,Cu3PP元素化合价由0价变为-3价,Cu元素化合价由+2价变为+1价,所以仅是还原产物,故B错误;
C.在反应②中,15molCuSO4转移30mol电子,则当有5mol CuSO4发生反应时,共转移10mol电子,故C正确;
D、反应①中CuSO4做氧化剂,反应②中CuSO4作氧化剂,故D错误;
故选C.
点评 本题考查氧化还原反应,明确元素化合价变化是解本题关键,注意该反应中P元素化合价变化,为易错点,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 期末集结号系列答案
期末集结号系列答案
相关题目
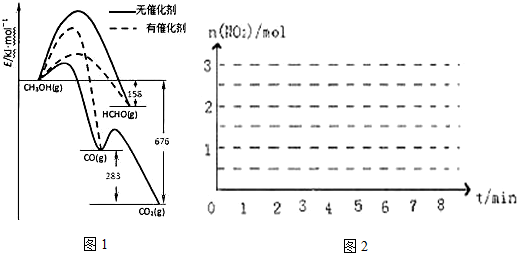
7.(1)(1)人们常用催化剂来选择反应进行的方向.如图1所示为一定条件下1mol CH3OH与O2发生反应时,生成CO、CO2或HCHO的能量变化图[反应物O2(g)和生成物H2O(g)略去].
①写出1mol HCHO与O2反应主要生成CO和H2O(g)的热化学方程式:HCHO(g)+$\frac{1}{2}$O2(g)═CO(g)+H2O(g)△H=-235kJ•mol-1.
②CH3OH与O2在有催化剂作用下反应,产物中HCHO比率大大提高的原因是催化剂使生成HCHO的活化能降低,同时使生成CO的活化能升高,并且生成HCHO的活化能低于生成CO的活化能.
(2)①一定温度下,将N2H4与NO2以体积比为1:1置于容积固定的容器中发生反应2N2H4(g)+2NO2(g)?3N2(g)+4H2O(Ⅰ)△H<0,下列能说明反应达到平衡状态的是AD.
A.混合气体密度保持不变B.2vg正(NO2)=2v正(N2)
C.N2H4与NO2体积比保持不变D.体系压强保持不变
②在某温度下,10L密闭容器中发生上述反应,容器内部分物质的物质的量变化如下表:
i.前2min内NO2的平均反应速率为0.025mol•L-1•min-1(保留2位有效数字,下同).
该温度下反应的平衡常数K8.4.
ii.关于上述反应,下列叙述不正确的是A.
A.达到平衡时,移走部分N2,平衡将向右移动,正反应速率加快
B.缩小容器的体积,平衡将向右移动,c(N2H2)将变大
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度和压强不变,再向容器中充入He,则此时v(逆)>v(正)
iii.请画出该反应中n(NO2)随时间变化曲线并画出在第7min时分别升温、加压的情况下n(NO2)随时间变化示意图(在图2上注明变化的条件).
①写出1mol HCHO与O2反应主要生成CO和H2O(g)的热化学方程式:HCHO(g)+$\frac{1}{2}$O2(g)═CO(g)+H2O(g)△H=-235kJ•mol-1.
②CH3OH与O2在有催化剂作用下反应,产物中HCHO比率大大提高的原因是催化剂使生成HCHO的活化能降低,同时使生成CO的活化能升高,并且生成HCHO的活化能低于生成CO的活化能.
(2)①一定温度下,将N2H4与NO2以体积比为1:1置于容积固定的容器中发生反应2N2H4(g)+2NO2(g)?3N2(g)+4H2O(Ⅰ)△H<0,下列能说明反应达到平衡状态的是AD.
A.混合气体密度保持不变B.2vg正(NO2)=2v正(N2)
C.N2H4与NO2体积比保持不变D.体系压强保持不变
②在某温度下,10L密闭容器中发生上述反应,容器内部分物质的物质的量变化如下表:
| 物质的量/mol 时间 | n(N2H4) | N(NO2) | N(N2) |
| 起始 | 2.0 | 3.0 | 0 |
| 第2min | 1.5 | a | 0.75 |
| 第4min | 1.2 | b | 1.2 |
| 第6min | 1.0 | c | 1.5 |
| 第7min | 1.0 | c | 1.5 |
该温度下反应的平衡常数K8.4.
ii.关于上述反应,下列叙述不正确的是A.
A.达到平衡时,移走部分N2,平衡将向右移动,正反应速率加快
B.缩小容器的体积,平衡将向右移动,c(N2H2)将变大
C.在相同的条件下,若使用甲催化剂能使正反应速率加快105倍,使用乙催化剂能使逆反应速率加快108倍,则应该选用乙催化剂
D.若保持平衡时的温度和压强不变,再向容器中充入He,则此时v(逆)>v(正)
iii.请画出该反应中n(NO2)随时间变化曲线并画出在第7min时分别升温、加压的情况下n(NO2)随时间变化示意图(在图2上注明变化的条件).

8.为研究铜与浓硫酸的反应,某化学兴趣小组进行如下实验.
实验I:反应产物的定性探究--按如图装置(固定装置已略)进行实验:
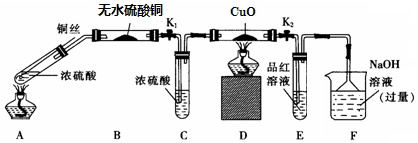
(1)F装置的烧杯中发生反应的离子方程式是SO2+2OH-=SO32-+H2O;
(2)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是D装置中黑色固体颜色无变化,E装置中溶液褪色
(3)实验结束时,撤去所有酒精灯之前必须完成的实验操作是拉起铜丝,关闭K1,K2
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是将A装置中试管内冷却后的混合物沿杯壁(或玻璃棒)缓缓倒入盛有水的烧杯中,并不断搅拌,若溶液变蓝,证明含有Cu2+;
,若溶液变蓝,证明含有Cu2+
实验Ⅱ:反应产物的定量探究
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,且黑色物质为Cu2S.产生Cu2S的反应为
aCu+bH2SO4$\frac{\underline{\;\;△\;\;}}{\;}$cCu2S+dCuSO4+e H2O,则a:b=5:4
(6)为进一步探究该黑色物质的成分,经查阅相关文献获得下列资料.
资料1:
资料2:X-射线晶体分析表明,铜与浓硫酸反应生成的黑色物质为Cu2S、CuS、Cu7S4中的一种或几种.仅由上述资料可得出的如下结论中正确是ABD.
A.铜与浓硫酸反应时所涉及的反应可能不止一个
B.硫酸浓度选择适当,可避免最后产物中出现黑色物质
C.该反应发生的条件之一是硫酸浓度≥15mol/L
D.硫酸浓度越大,黑色物质越快出现、越难消失.
实验I:反应产物的定性探究--按如图装置(固定装置已略)进行实验:

(1)F装置的烧杯中发生反应的离子方程式是SO2+2OH-=SO32-+H2O;
(2)实验过程中,能证明浓硫酸中硫元素的氧化性强于氢元素的现象是D装置中黑色固体颜色无变化,E装置中溶液褪色
(3)实验结束时,撤去所有酒精灯之前必须完成的实验操作是拉起铜丝,关闭K1,K2
(4)实验结束后,证明A装置试管中反应所得产物是否含有铜离子的操作方法是将A装置中试管内冷却后的混合物沿杯壁(或玻璃棒)缓缓倒入盛有水的烧杯中,并不断搅拌,若溶液变蓝,证明含有Cu2+;
,若溶液变蓝,证明含有Cu2+
实验Ⅱ:反应产物的定量探究
(5)在铜与浓硫酸反应的过程中,发现有黑色物质出现,且黑色物质为Cu2S.产生Cu2S的反应为
aCu+bH2SO4$\frac{\underline{\;\;△\;\;}}{\;}$cCu2S+dCuSO4+e H2O,则a:b=5:4
(6)为进一步探究该黑色物质的成分,经查阅相关文献获得下列资料.
资料1:
| 硫酸/mol•L-1 | 黑色物质出现的温度/℃ | 黑色物质消失的温度/℃ |
| 14 | Cu 片表面无明显现象 | |
| 15 | 约150 | 约236 |
| 16 | 约140 | 约250 |
| 18 | 约120 | 不消失 |
A.铜与浓硫酸反应时所涉及的反应可能不止一个
B.硫酸浓度选择适当,可避免最后产物中出现黑色物质
C.该反应发生的条件之一是硫酸浓度≥15mol/L
D.硫酸浓度越大,黑色物质越快出现、越难消失.
12.炼金废水中所含CN-有剧毒,其性质与卤素离子相似,还原性介于I-与Br-之间,HCN为弱酸.下列说法不正确的是( )
| A. | CN-可以和稀硫酸反应生成HCN | B. | CN-可被Cl2氧化成(CN)28 | ||
| C. | 在水溶液中(CN)2可被F-还原 | D. | HCN的电子式为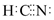 |
2.下列实验操作能达到相应实验目的是
| 诜项 | 实验操作 | 实验目的 |
| A | 将乙烯通入酸性KMnO4溶液中 | 证明乙烯能发生加成反应 |
| B | 向含酚酞的NaOH溶液中加入氯水 | 证明Cl2具有漂白性 |
| C | 常温下,向Fe和Cu中分别加入浓硝酸 | 比较Fe和Cu的金属活动性 |
| D | 将铁钉放入试管中,下端浸入食盐水中 | 验证铁的吸氧腐蚀 |
| A. | A | B. | B | C. | C | D. | D |
5.下列离子方程式中,正确的是( )
| A. | Na2O2溶于水产生O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| B. | 钠与CuSO4溶液反应:2Na+Cu2+═Cu↓+2Na+ | |
| C. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O | |
| D. | Ba(OH)2溶液与稀H2SO4反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O |
4.己知元素X、Y同周期,且电负性X>Y,下列说法中一定不正确的是( )
| A. | 第一电离能:Y<X | |
| B. | 最简单气态氢化物的稳定性:HmY>HnX | |
| C. | 最高价含氧酸的酸性:元素X对应酸的酸性强于Y | |
| D. | X和Y形成的化合物中,X显负价,Y显正价 |
 A、B、C、D、E五种元素中只有E为金属元素,五种元素的原子叙述按B、D、C、A、E的顺序依次增大,D、C元素在元素周期表中位置相邻,在一定条件下,B的单质可以分别和A、.C、D的单质化合生成甲、乙、丙化合物,C的单质和D的单质化合物可得丁,戊、己、庚均为化合物.已知乙、丙每个分子中均含有10个电子,图为相互转化关系.
A、B、C、D、E五种元素中只有E为金属元素,五种元素的原子叙述按B、D、C、A、E的顺序依次增大,D、C元素在元素周期表中位置相邻,在一定条件下,B的单质可以分别和A、.C、D的单质化合生成甲、乙、丙化合物,C的单质和D的单质化合物可得丁,戊、己、庚均为化合物.已知乙、丙每个分子中均含有10个电子,图为相互转化关系.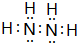 .
.