题目内容
下列说法正确的是( )
| A、沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
| B、KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| C、根据是否有丁达尔效应将分散系分为溶液、胶体和浊液 |
| D、使用静电除尘器除去空气中的飘尘利用了胶体的性质 |
考点:分散系、胶体与溶液的概念及关系,胶体的重要性质,电解质与非电解质
专题:
分析:A、胶体是中性的分散系,不带电荷,胶体微粒能吸附带电粒子;
B、溶于水自身能电离出离子的化合物为电解质;
C、分散系是依据分散质微粒直径大小分类;
D、静电出除尘利用胶体微粒吸附带电粒子,通电向某极移动,是胶体的电泳.
B、溶于水自身能电离出离子的化合物为电解质;
C、分散系是依据分散质微粒直径大小分类;
D、静电出除尘利用胶体微粒吸附带电粒子,通电向某极移动,是胶体的电泳.
解答:
解:A、胶体是中性的分散系,不带电荷,胶体微粒能吸附带电粒子导电,故A错误;
B、溶于水自身能电离出离子的化合物为电解质,SO3不能电离出离子是非电解质,故B错误;
C、分散系是依据分散质微粒直径大小分类,丁达尔现象是胶体的性质,故C错误;
D、静电出除尘利用胶体微粒吸附带电粒子,通电向某极移动,是胶体的电泳现象的应用,故D正确;
故选D.
B、溶于水自身能电离出离子的化合物为电解质,SO3不能电离出离子是非电解质,故B错误;
C、分散系是依据分散质微粒直径大小分类,丁达尔现象是胶体的性质,故C错误;
D、静电出除尘利用胶体微粒吸附带电粒子,通电向某极移动,是胶体的电泳现象的应用,故D正确;
故选D.
点评:本题考查了胶体性质分析,分散系的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
下列说法中错误的是( )
| A、在NH4+和Fe(CO)5中都存在配位键 |
| B、SO2、SO3都是极性分子 |
| C、元素电负性越大的原子,该元素的原子吸引电子的能力越强 |
| D、离子晶体的晶格能随着离子间距的减少而增大,晶格能越大,晶体的熔点越高 |
下列图象表达正确的是( )

| A、浓硫酸的稀释 |
| B、过量的盐酸与等量的锌粉反应 |
| C、氢气与氧气反应中的能量变化 |
| D、微粒电子数 |
下列俗名与化学式对应的是( )
| A、石膏:CaSO4?2H2O |
| B、碳铵:(NH4)2CO3 |
| C、重晶石:BaCO3 |
| D、芒硝:Na2SO4?12H2O |
将标准状况下密度为ρg/L的HCl气体V L溶于1000g水中,得到密度为b g/cm3的盐酸,则该盐酸的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
将钠投入到滴有酚酞的水中,下列有关叙述中不正确的是( )
| A、产生无色气体 |
| B、Na下沉 |
| C、溶液变红 |
| D、Na块熔化成小球 |
某有机物的氧化产物是甲,还原产物是乙.甲和乙都能与钠反应放出H2,甲和乙反应生成丙,甲和丙都能发生银镜反应.该有机物是( )
| A、甲醛 | B、乙醛 | C、甲酸 | D、甲醇 |
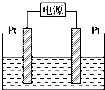 熔融盐燃料电池具有较高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2-和HCO)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池负极电极反应式为:2C4H10+26CO-52e-═34CO2+10H2O.
熔融盐燃料电池具有较高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2-和HCO)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池负极电极反应式为:2C4H10+26CO-52e-═34CO2+10H2O.