题目内容
 熔融盐燃料电池具有较高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2-和HCO)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池负极电极反应式为:2C4H10+26CO-52e-═34CO2+10H2O.
熔融盐燃料电池具有较高的发电效率,因而受到重视.某燃料电池以熔融的K2CO3(其中不含O2-和HCO)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极.该燃料电池负极电极反应式为:2C4H10+26CO-52e-═34CO2+10H2O.试回答下列问题:
(1)该燃料电池的化学反应方程式为
(2)正极电极反应式为
(3)为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定.为此,必须在通入的空气中加入一种物质,加入的物质是
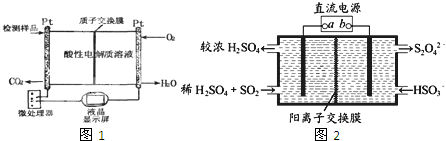
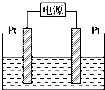
(4)某学生想用该燃料电池和如图所示装置电解饱和食盐水:写出反应的离子方程式
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)丁烷和氧气反应生成二氧化碳和水;
(2)正极上氧气得电子发生还原反应;
(3)根据碳守恒和两极上的变化考虑;
(4)电解饱和食盐水时,阳极上氯离子放电,阴极上氢离子放电,生成氢气、氯气和氢氧化钠.
(2)正极上氧气得电子发生还原反应;
(3)根据碳守恒和两极上的变化考虑;
(4)电解饱和食盐水时,阳极上氯离子放电,阴极上氢离子放电,生成氢气、氯气和氢氧化钠.
解答:
解:(1)该电池中,丁烷和氧气反应生成二氧化碳和水,反应方程式为:2C4H10+13O2=8CO2+10H2O,
故答案为:2C4H10+13O2═8CO2+10H2O;
(2)正极上氧气得电子发生还原反应和二氧化碳反应生成碳酸根离子,电极反应式为:O2+2CO2+4e-=2CO32-
故答案为:O2+2CO2+4e-═2CO32-;
(3)由于原电池的负极产物有水生成,所以负极必有CO32-参加反应,同时根据碳守恒可知A必为CO2,负极反应式可表示为CH4+4CO32--8e-=5CO2+2H2O,故答案为:CO2;
(4)电解饱和食盐水时,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,同时还生成氢氧化钠,离子方程式为2Cl-+2H2O
Cl2↑+H2↑+2OH-,
故答案为:2Cl-+2H2O
Cl2↑+H2↑+2OH-.
故答案为:2C4H10+13O2═8CO2+10H2O;
(2)正极上氧气得电子发生还原反应和二氧化碳反应生成碳酸根离子,电极反应式为:O2+2CO2+4e-=2CO32-
故答案为:O2+2CO2+4e-═2CO32-;
(3)由于原电池的负极产物有水生成,所以负极必有CO32-参加反应,同时根据碳守恒可知A必为CO2,负极反应式可表示为CH4+4CO32--8e-=5CO2+2H2O,故答案为:CO2;
(4)电解饱和食盐水时,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,同时还生成氢氧化钠,离子方程式为2Cl-+2H2O
| ||
故答案为:2Cl-+2H2O
| ||
点评:本题考查了原电池原理,为高频考点,侧重于学生的分析能力的考查,明确正负极上得失电子的物质是解本题关键,注意把握电极方程式的书写,难度中等.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
某稀溶液中含4mol KNO3和2.5mol H2SO4,向其中加入1.5mol铁,充分反应后产生的NO气体在标准状况下的体积为( )
| A、36L | B、22.4L |
| C、28L | D、11.2L |
当溶液中有大量的H+和Ba2+时,下列离子中有可能大量存在的是( )
| A、SO42- |
| B、CO32- |
| C、Cl- |
| D、OH- |
下列各组离子在无色透明的酸性溶液中能大量共存的是( )
| A、Fe3+、HCO3-、Cl-、Na+ |
| B、SO42-、NO3-、Ba2+、Cu2+ |
| C、MnO4-、Na+、K+、Mg2+ |
| D、Ca2+、Cl-、NO3-、Na+ |
根据以下反应判断:Fe3+、Fe2+、Cu2+的氧化性强弱顺序是( )
①Fe+CuCl2=Cu+FeCl2
②2FeCl3+Cu=CuCl2+2FeCl2.
①Fe+CuCl2=Cu+FeCl2
②2FeCl3+Cu=CuCl2+2FeCl2.
| A、Fe2+>Cu2+>Fe3+ |
| B、Fe3+>Fe2+>Cu2+ |
| C、Fe3+>Cu2+>Fe2+ |
| D、Cu2+>Fe2+>Fe3+ |
某溶液中存在大量的H+、NO3-、Cl-,该溶液中还可能大量存在的离子是( )
| A、CO32- |
| B、OH- |
| C、Ag+ |
| D、SO42- |
下列说法正确的是( )
| A、沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
| B、KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| C、根据是否有丁达尔效应将分散系分为溶液、胶体和浊液 |
| D、使用静电除尘器除去空气中的飘尘利用了胶体的性质 |