题目内容
将标准状况下密度为ρg/L的HCl气体V L溶于1000g水中,得到密度为b g/cm3的盐酸,则该盐酸的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
考点:物质的量浓度的相关计算
专题:物质的量浓度和溶解度专题
分析:根据n=
计算氯化氢的物质的量,再m=nM计算氯化氢质量,溶液的质量=1000g+m(HCl),根据V=
求出溶液的体积,再根据c=
计算溶液的物质的量浓度;
或者根据m=ρV计算HCl的质量,进而计算溶液质量分数,再利用c=
计算溶液物质的量浓度.
| V |
| Vm |
| m |
| ρ |
| n |
| V |
或者根据m=ρV计算HCl的质量,进而计算溶液质量分数,再利用c=
| 1000ρω |
| M |
解答:
解:将标准状况下的V L HCl(气)的物质的量为
=
mol.
氯化氢的质量为
mol×36.5g/mol=
g.
所以溶液质量为1000g+
g=(1000+
)g.
所以溶液的体积为
=
L.
所以溶液浓度为
=
mol/L.
或者溶液质量为(1000+ρV)g,溶液质量分数=
,利用c=
可知,溶液物质的量浓度为
mol/L=
mol/L
故选:D.
| VL |
| 22.4L/mol |
| V |
| 22.4 |
氯化氢的质量为
| V |
| 22.4 |
| 36.5V |
| 22.4 |
所以溶液质量为1000g+
| 36.5V |
| 22.4 |
| 36.5V |
| 22.4 |
所以溶液的体积为
(1000+
| ||
| 1000bg/L |
| 22400+36.5V |
| 22400b |
所以溶液浓度为
| ||
|
| 1000bV |
| 22400+36.5V |
或者溶液质量为(1000+ρV)g,溶液质量分数=
| ρV |
| 1000+ρV |
| 1000ρω |
| M |
1000×b×
| ||
| 36.5 |
| 1000bρV |
| 36500+36.5ρV |
故选:D.
点评:本题考查物质的量浓度的相关计算,难度不大,正确判断溶液的体积是解本题的关键,注意不能把溶剂的体积当做溶液的体积,注意理解掌握质量分数与物质的量浓度之间关系.

练习册系列答案
相关题目
下列说法正确的是( )
| A、S2-电子排布式 1s22s22p63s23p4 |
| B、在金属晶体中,自由电子与金属离子或金属原子的碰撞有能量传递,可以用此来解释的金属的物理性质是导热性 |
| C、金属键可以看做是许多原子共用许多电子所形成的强烈相互作用,所以和共价键类似,也有饱和性和方向性 |
D、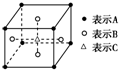 某物质的晶体中含A、B、C三种元素,其排列方式如图所示,晶胞中A、B、C的原子个数比为1:2:2. |
下列描述正确的是( )
| A、HCl和NaOH反应的中和热△H=-57.3kJ/mol,则NaOH和CH3COOH反应的中和热△H=-57.3kJ/mol |
| B、需要加热才能发生的反应一定是吸热反应 |
| C、CO(g)的燃烧热是-283.0kJ/mol,则2CO(g)+O2(g)=2CO2(g)反应的△H=-2×283.0kJ/mol |
| D、1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷燃烧热 |
下列说法正确的是( )
| A、沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
| B、KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| C、根据是否有丁达尔效应将分散系分为溶液、胶体和浊液 |
| D、使用静电除尘器除去空气中的飘尘利用了胶体的性质 |
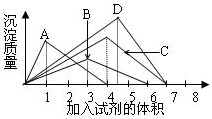 如图纵坐标表示沉淀的质量,横坐标表示所加试剂的体积,请选出有对应曲线变化关系的实验项( )
如图纵坐标表示沉淀的质量,横坐标表示所加试剂的体积,请选出有对应曲线变化关系的实验项( )| A、硝酸银溶液中加入氨水溶液 |
| B、往澄清石灰水中逐渐通入CO2气体 |
| C、往AlCl3溶液中逐NaOH溶液 |
| D、往NaAlO2溶液中逐滴加入盐酸溶液 |
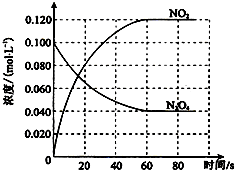 在容积为100L的容器中,通入一定量的N2O4,发生反应N2O4g)═2NO2 (g),随温度升高,混合气体的颜色变深.
在容积为100L的容器中,通入一定量的N2O4,发生反应N2O4g)═2NO2 (g),随温度升高,混合气体的颜色变深.