题目内容
8.下列实验能获得成功的是( )| A. | 苯和浓溴水用铁做催化剂制溴苯 | |
| B. | 将苯与浓硝酸和浓硫酸的混合酸共热至50℃~60℃制硝基苯 | |
| C. | 甲烷与氯气光照制得纯净的一氯甲烷 | |
| D. | 乙烯通入溴的四氯化碳溶液得到1,2-二溴乙烷 |
分析 A.苯与溴水不反应;
B.苯与浓硝酸和浓硫酸的混合酸在水浴加热下发生取代反应生成硝基苯;
C.光照下取代反应为链锁反应,产物复杂,且一氯甲烷中可能混有甲烷或氯气;
D.乙烯与溴发生加成反应生成1,2-二溴乙烷,易溶于四氯化碳.
解答 解:A.苯与溴水不反应,应选苯和液溴、用铁做催化剂制溴苯,故A错误;
B.苯与浓硝酸和浓硫酸的混合酸在水浴50℃~60℃下发生取代反应生成硝基苯,方案合理,故B正确;
C.光照下取代反应为链锁反应,产物复杂,且一氯甲烷中可能混有甲烷或氯气,应选乙烯与HCl发生加成反应制备,故C错误;
D.乙烯与溴发生加成反应生成1,2-二溴乙烷,易溶于四氯化碳,应选乙烯与单质溴发生加成反应制备,故D错误;
故选B.
点评 本题考查有机物的制备实验评价,为高频考点,把握有机物的性质、有机反应等为解答的关键,侧重分析与应用能力的考查,注意制备产物要纯净、方案要合理,题目难度不大.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
4.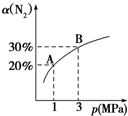 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )
 某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )
某温度下,对于反应N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol,N2的平衡转化率(α)与体系总压强(p)的关系如图所示.下列说法正确的是( )| A. | 平衡状态由A变到B时,平衡常数K(A)=K(B) | |
| B. | 将1 mol氮气、3 mol氢气,置于1 L密闭容器中发生反应,放出的热量为92.4 kJ | |
| C. | 升高温度,逆反应速率增大,正反应速率减小 | |
| D. | 上述反应达到平衡后,增大H2浓度,平衡正向移动,H2转化率增大 |
19.下列反应不能通过一步反应实现的是( )
| A. | SiO2→H2SiO3 | B. | Cu→CuSO4 | C. | Fe→FeCl2 | D. | Al→Na[Al(OH)4] |
3.已知醚类物质不能与Na、K等金属单质发生化学反应.现知二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是( )
| A. | 利用金属钠或者金属钾 | B. | 利用质谱法 | ||
| C. | 利用红外光谱法 | D. | 利用核磁共振氢谱 |
13.酸具有共同的性质,是因为( )
| A. | 都能电离出氢离子 | B. | 都能使石蕊试液变红 | ||
| C. | 都能跟碱反应生成盐和水 | D. | 都含有氧元素 |
17.在pH=1的澄清透明溶液中,不能大量共存的离子组是( )
| A. | Na+、K+、NO3-、CO32- | B. | Cu2+、NH4+、SO42-、Cl- | ||
| C. | Ba2+、K+、Cl-、Br- | D. | Zn2+、Na+、NO3-、SO42- |
18.下列离子方程式正确的是( )
| A. | 将过量SO2通入稀氨水中:SO2+NH3•H2O=HSO3-+NH4+ | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| C. | 大理石溶于醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| D. | AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O=AlO2-+4NH4++2H2O |
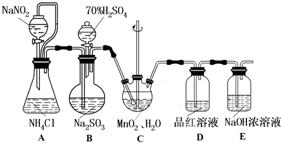
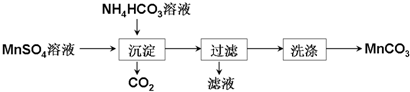
 ;元素Z的离子结构示意图为
;元素Z的离子结构示意图为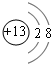 .
.