题目内容
14.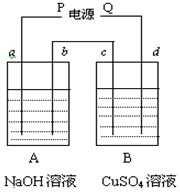 按如图装置实验,a、b、c、d均为惰性电极,A、B两烧杯中分别盛放NaOH溶液和足量CuSO4溶液.通电一段时间后,c电极质量增加6.4g,试回答:
按如图装置实验,a、b、c、d均为惰性电极,A、B两烧杯中分别盛放NaOH溶液和足量CuSO4溶液.通电一段时间后,c电极质量增加6.4g,试回答:(1)电源Q为正极;
(2)b极产生气体的体积为1.12L(标准状况);电解一段时间后,A池中溶液的PH变大.(填“变大”“变小”或“不变”)
(3)d极上所发生的电极反应式:4OH--4e-=2H2O+O2↑.
(4)B装置中电解反应的离子方程式为:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$ 2Cu+O2↑+4H+.
分析 (1)电解池中,电极质量增加的极是阴极,和电源的负极相连的是阴极,和电源的正极相连的是正极,据此来判断;
(2)整个电路是串联的,所以每个烧杯中的电极上转移电子数是相等的,据电极反应和电子守恒来计算;根据电解的实质是电解水以及溶液浓度的变化情况来回答;(3)d是阳极,电解硫酸铜时,在阳极上是氢氧根离子放电,电极反应式为:4OH--4e-=2H2O+O2↑,
(4)B装置中总的电解原理方程式为:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4,离子方程式为:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$ 2Cu+O2↑+4H+.
解答 解:(1)B杯中c质量增加,说明Cu沉积在c电极上,所以c是阴极,d是阳极,即Q为正极,P为负极,故答案为:正;
(2)P是负极,所以a是阴极,b是阳极,b极上的电极反应为:4OH--4e-=2H2O+O2↑,c极上的电极反应为:Cu2++2e-=Cu,整个电路是串联的,所以每个烧杯中的电极上转移电子数是相等的,据电极反应:Cu2++2e-=Cu,可知c极上有6.4gCu析出,转移0.2mol电子,当转移0.2mol电子时,b极上生成氧气的物质的量为0.05mol,体积为0.05mol×22.4L/mol=1.12L,A烧杯溶液电解的实质是电解水,所以氢氧化钠溶度增大,PH变大,故答案为:1.12;变大;
(3)d是阳极,电解硫酸铜时,在阳极上是氢氧根离子放电,电极反应式为:4OH--4e-=2H2O+O2↑,故答案为:4OH--4e-=2H2O+O2↑;
(4)B装置中总的电解原理方程式为:2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4,离子方程式为:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$ 2Cu+O2↑+4H+,故答案为:2Cu2++2H2O$\frac{\underline{\;通电\;}}{\;}$ 2Cu+O2↑+4H+.
点评 本题为电化学知识的综合应用,做题时要注意根据电极反应现象判断出电解池的阴阳级,进而判断出电源的正负极,要注意三个电解池为串联电路,各电极上得失电子的数目相等.做题时要正确写出电极方程式,准确判断两极上离子的放电顺序.

 走进文言文系列答案
走进文言文系列答案| A. | AlCl3与NH3•H2O | B. | NaOH与CO2 | C. | Na2CO3与HCl | D. | Na与O2 |
| A. | 500 ml,1mol/LFe2(SO4)3溶液和250mL 3mol/L的Na2SO4溶液所含硫酸根离子的物质的量浓度相等 | |
| B. | 若R的含氧酸的酸性大于Q的含氧酸的酸性,则非金属性R大于Q | |
| C. | 1.2gNaHSO4晶体中阳离子和阴离子的总数为0.03NA | |
| D. | 含NA个Na+的Na2O溶解于1L水中.Na+的物质的量浓度为lmol/L |
| A. | 溶液、胶体和悬浊液三种分散系的本质区别是分散质微粒直径的大小 | |
| B. | 甲醇和氧气以及KOH溶液构成的新型燃料电池中,其正极上发生的反应为:CH3OH-6e-+8OH-=CO32-+6H2O | |
| C. | 在铁上镀铜时,金属铜作阴极 | |
| D. | 电解法精炼铜时,电解质溶液中铜离子浓度一定不变 |
| A. | 1.0×l0-15 | B. | 1.0×10-14 | C. | 1.0×10-13 | D. | l.0×l0-7 |
| A. | 明矾可以除去水中的悬浮颗粒等杂质,所以可以作净水剂 | |
| B. | 可用燃烧的方法鉴别羊毛围巾和合成纤维围巾 | |
| C. | 黄瓜含有丰富的维生素C,热锅爆炒可以减少维生素C的流失 | |
| D. | 石英玻璃纤维传导光的能力非常强,所以常用于制作光纤 |
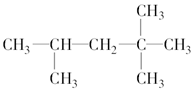 2,2,4-三甲基戊烷
2,2,4-三甲基戊烷 3,4-二甲基己烷
3,4-二甲基己烷