题目内容
下列关于氯水的叙述不正确的是( )
| A、新制的氯水可使干燥的有色布条褪色 |
| B、新制的氯水呈黄绿色是因为在溶液中溶有氯气分子 |
| C、与久置氯水不同,在新制氯水中加入硝酸银溶液后无白色沉淀 |
| D、氯水久置后,会使溶液酸性增强 |
考点:氯、溴、碘及其化合物的综合应用
专题:
分析:氯水中,氯气与水发生:Cl2+H2O?HClO+HCl,溶液中含有Cl2、HClO、H2O等分子,含有H+、ClO-、Cl-等离子,氯水具有酸性和强氧化性,其中HClO见光易分解生成盐酸而变质,以此解答.
解答:
解:A、含HClO的物质能使干燥的有色布条褪色,氯水中含有Cl2、HClO、H2O等分子,可使干燥的有色布条褪色,故A正确;
B、新制的氯水中含有Cl2、HClO、H2O等分子,是溶液呈黄绿色,故B正确;
C、在新制氯水中含有H+、ClO-、Cl-等离子,加入硝酸银溶液后生成白色沉淀氯化银,故C错误;
D、氯水久置后,HClO见光易分解生成盐酸而变成盐酸溶液,使溶液酸性增强,故D正确.
故选:C.
B、新制的氯水中含有Cl2、HClO、H2O等分子,是溶液呈黄绿色,故B正确;
C、在新制氯水中含有H+、ClO-、Cl-等离子,加入硝酸银溶液后生成白色沉淀氯化银,故C错误;
D、氯水久置后,HClO见光易分解生成盐酸而变成盐酸溶液,使溶液酸性增强,故D正确.
故选:C.
点评:本题综合考查氯气和氯水的性质,注意把握氯气和水反应的特点以及氯水的成分和性质,为高考高频考点,侧重于基础知识的综合运用,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
将几滴KSCN(SCN-是“类卤离子”,与氯离子性质相似)溶液加入酸性的含有Fe3+的溶液中,溶液变成血红色.将该红色溶液分为两份,①一份中加入适量KMnO4溶液,红色褪去;②向另一份中通入SO2,红色也褪去.下列说法不正确的是( )
| A、①红色褪去的原因可能是KMnO4将SCN-氧化,使[Fe(SCN)]2+消失 |
| B、[Fe(SCN)]2+中Fe3+与SCN-以配位键结合 |
| C、②红色褪去的原因是SO2具有还原性 |
| D、SCN-在适当条件下可被还原为(SCN)2 |
某烃结构式如下:CH3- -C≡C-CH=CH-CH3,有关其结构说法正确的是( )
-C≡C-CH=CH-CH3,有关其结构说法正确的是( )
 -C≡C-CH=CH-CH3,有关其结构说法正确的是( )
-C≡C-CH=CH-CH3,有关其结构说法正确的是( )| A、该分子中有6个碳原子一定在同一条直线上 |
| B、该分子中有8个碳原子可能在同一条直线上 |
| C、该分子中所有碳原子一定都在同一平面上 |
| D、该分子中所有氢原子可能在同一平面 |
在AgNO3、Cu(NO3)2和Zn(NO3)2混合溶液中,加入一定量的铁粉,充分反应后过滤,在滤渣中加入稀盐酸,有气体产生.则下列结论正确的是( )
| A、滤液中一定有Fe(NO3)3 |
| B、滤渣只含Ag和Cu,一定无Zn |
| C、滤渣中一定有Ag、Cu和Fe,一定无Zn |
| D、滤渣中可能有Ag、Cu、Fe和Zn |
下列说法正确的是( )
| A、CO2的水溶液能导电,所以CO2是电解质 |
| B、氧化剂在反应中得到的电子越多,氧化能力越强 |
| C、用加热法可分离I2和NH4HCO3两种固体 |
| D、Cl2的氧化性比I2强,而I-的还原性却比Cl-强 |
使5.6LCO2气体迅速通过Na2O2固体后得到4.48L气体(标准状况),4.48L气体的质量是( )
| A、8.8 g |
| B、8.2 g |
| C、6.4 g |
| D、11g |
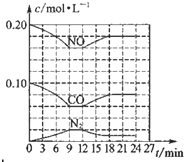 将0.20mol NO和0.1mol CO充入一个容积恒定为1L的密闭容器中发生反应:2NO(g)+2CO(g)═N2(g)+2CO2(g)△H<0在不同条件下,反应过程中部分物质的浓度变化如图所示.下列说法正确的是( )
将0.20mol NO和0.1mol CO充入一个容积恒定为1L的密闭容器中发生反应:2NO(g)+2CO(g)═N2(g)+2CO2(g)△H<0在不同条件下,反应过程中部分物质的浓度变化如图所示.下列说法正确的是( )| A、容器内的压强不发生变化说明该反应达到平衡 |
| B、当向容器中再充入0.20 mol NO时,平衡向正反应方向移动,K增大 |
| C、第12 min时改变的反应条件为减小压强 |
| D、向该容器内充入He气,容器内气体压强增大,所以反应速率增大 |
 分馏又称为分级蒸馏或精馏.适用于互溶而且沸点相差很小的多组分混合液的分离.控制好温度,便可将各种物质分离.有关分馏操作,下列说法正确的是( )
分馏又称为分级蒸馏或精馏.适用于互溶而且沸点相差很小的多组分混合液的分离.控制好温度,便可将各种物质分离.有关分馏操作,下列说法正确的是( )