题目内容
下列说法正确的是( )
| A、CO2的水溶液能导电,所以CO2是电解质 |
| B、氧化剂在反应中得到的电子越多,氧化能力越强 |
| C、用加热法可分离I2和NH4HCO3两种固体 |
| D、Cl2的氧化性比I2强,而I-的还原性却比Cl-强 |
考点:电解质与非电解质,氧化性、还原性强弱的比较,物质的分离、提纯的基本方法选择与应用
专题:
分析:A、CO2的水溶液能导电的原因是碳酸发生电离,二氧化碳不能发生电离,CO2是非电解质;
B、氧化剂在反应中越易得电子,氧化能力越强;
C、碳酸氢铵受热分解,碘受热升华;
D、根据“易得不易失”分析.
B、氧化剂在反应中越易得电子,氧化能力越强;
C、碳酸氢铵受热分解,碘受热升华;
D、根据“易得不易失”分析.
解答:
解:A、CO2的水溶液能导电的原因是碳酸发生电离,二氧化碳不能发生电离,CO2是非电解质,故A错误;
B、氧化性的强弱与得电子多少无关,氧化剂在反应中越易得电子,氧化能力越强,故B错误;
C、碳酸氢铵受热分解,碘受热升华,加热时变为气体,不能实现二者的分离,故C错误;
D、氧化性:Cl2>I2,说明Cl2比I2易得电子,则Cl-相对于I-不易失电子,即为还原性:Cl-<I-,故D正确;
故选D.
B、氧化性的强弱与得电子多少无关,氧化剂在反应中越易得电子,氧化能力越强,故B错误;
C、碳酸氢铵受热分解,碘受热升华,加热时变为气体,不能实现二者的分离,故C错误;
D、氧化性:Cl2>I2,说明Cl2比I2易得电子,则Cl-相对于I-不易失电子,即为还原性:Cl-<I-,故D正确;
故选D.
点评:本题考查问题较为全面,涉及电解质和非电解质的区分、氧化性和还原性的比较、物质分离和提纯等知识,为高频考点,难度不大,注意氧化还原反应理论的学习.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在乙醇发生的各种反应中,断键方式不正确的是( )
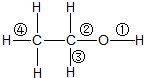

| A、与金属钠反应时,键①断裂 |
| B、与醋酸、浓硫酸共热时,键②断裂 |
| C、与HCl反应生成氯乙烷时,键②断裂 |
| D、与浓硫酸共热至170℃时,键②和④断裂 |
下列关于氯水的叙述不正确的是( )
| A、新制的氯水可使干燥的有色布条褪色 |
| B、新制的氯水呈黄绿色是因为在溶液中溶有氯气分子 |
| C、与久置氯水不同,在新制氯水中加入硝酸银溶液后无白色沉淀 |
| D、氯水久置后,会使溶液酸性增强 |
下列各组中的离子,能在溶液中大量共存的是( )
| A、Na+、H+、Cl-、CO32- |
| B、Na+、Ca2+、CO32-、NO3- |
| C、Na+、Ca2+、Cl-、NO3- |
| D、K+、H+、SO42-、OH- |
关于1mol?L-1CaCl2溶液的下列说法正确的是( )
| A、溶液中c(Cl-)=2 mol?L-1 |
| B、由1mol CaCl2溶于1L水中制得 |
| C、溶液中含有1mol CaCl2 |
| D、1L 溶液中含2molCa2+,2mol Cl- |
下列变化属于氧化反应的是( )
| A、CO2→CO |
| B、Cl-→Cl2 |
| C、Fe3+→Fe2+ |
| D、CO32-→CO2 |
最近江苏省大部分地区遭受严重的雾霾天气,雾霾属于哪种分散系( )
| A、溶液 | B、胶体 |
| C、乳浊液 | D、悬浊液 |