题目内容
如图是某研究小组采用电解法处理石油炼制过程中产生的大量H2S废气的工艺流程。该方法对H2S的吸收率达99%以上,并可制取H2和S。下列说法正确的是
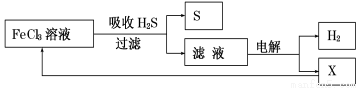
A.吸收H2S的离子方程式为:2Fe3++H2S =2Fe2++S↓+2H+
B.电解时选用阴离子交换膜,电解过程中的阳极区反应主要为:2Cl--2e- = Cl2
C.电解过程中若阴极产生2.24L气体,则阳极区产生0.2mol Fe3+
D.实验室可用点燃充分燃烧的方法消除H2S污染
A
【解析】
试题分析:A、由图中的流程图可知,FeCl3与H2S反应生成S和Fe2+,离子方程式正确,得失电子数是守恒的,故A正确;B、电解的是氯化亚铁和盐酸溶液,阳极发生的应该是氧化反应,所得滤液中含有Fe2+、H+和Cl-,由于还原性Fe2+>Cl-(或根据图示循环),电解时阳极反应式为Fe2+-e-=Fe3+,故B错误;C、不能起到H2S的状态,不能计算其物质的量,故C不正确;D、由于H2S充分燃烧的化学方程式为2H2S+3O2=2SO2+2H2O,生成的SO2也是一种有毒气体,故D错误,故选:A。
考点:考查离子方程式正误判断,电极反应式的书写,H2S的化学性质

(每空2分,共12分)
PCl3与PCl5均是有机合成的重要中间体,两者存在以下相互转化关系:
PCl5(g)  PCl3(g) + Cl2(g) △H=a kJ·mol-1 在210℃时,将4mol PCl5气体充入
PCl3(g) + Cl2(g) △H=a kJ·mol-1 在210℃时,将4mol PCl5气体充入
2L真空密闭容器中发生上述反应,得到如下数据:
时间(s) | 0 | 20 | 40 | 60 |
n(PCl5) | 4 | 2.8 | 2 | 2 |
(1)已知上述反应在温度较高时才能自发进行,则a 0(填﹥、﹦、﹤);
(2)计算从20s至40s共20s的时间内,用PCl3表示的平均反应速率为 。210℃时该反应的平衡常数K值等于 。
(3)反应进行至60s后,将混合物的温度降低,重新达到平衡后氯气浓度将 (填“增大”、“减少”或“不变”)。
(4)欲增大该反应的K值,可采取的措施有(填序号)
A.降低温度 B.向混合气体中通入Cl2
C.使用高效催化剂 D.升高温度
(5)如右图是210℃时容器中PCl5物质的量的变化曲线,请在该图中补画出该反应在160℃时PCl5物质的量的变化曲线。