题目内容
W、X、Y、Z均是短周期元素,X、Y处于同一周期,X、Z的最低价离子分别为 X2- 和
Z- ,Y+ 和Z- 离子具有相同的电子层结构。下列说法正确的是( )
A. 原子最外层电子数:X>Y>Z B. 单质沸点:X>Y>Z
C. 离子半径:X2->Y+>Z- D. 原子序数:X>Y>Z
D
【解析】
试题分析:X、Z的最低价离子分别为X2-和Z-,则X为第ⅥA族元素,Z为ⅦA族元素;Y+和Z-具有相同的电子层结构,则Y在Z的下一周期,则Y为Na元素,Z为F元素,X、Y同周期,则X为S元素。A、X、Y、Z分别为S、Na、F,原子最外层电子数分别为6、1、7,故A错误;B、常温下Na、S为固体,F2为气体,Na的熔点较低,但钠的沸点高于硫,顺序应为Na>S>F2,故B错误;C、Na+、F-具有相同的核外电子排布,离子的核电荷数越大,半径越小,应为F->Na+,故C错误;D、X、Y、Z原子序数分别为16、11、9,原子序数:X>Y>Z,故D正确。
考点:本题考查原子结构与元素周期律。

练习册系列答案
相关题目
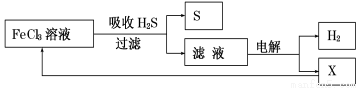
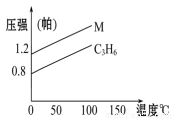
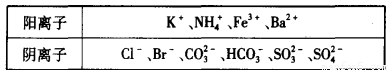
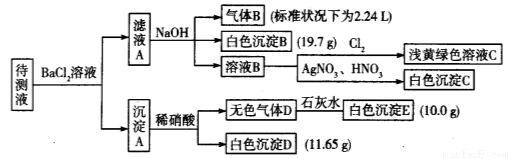
 NH3↑+H2O
NH3↑+H2O