题目内容
下列各组物质的性质比较,正确的是
A.稳定性:H2O<NH3<PH3<SiH4
B.熔点:CO2<H2O<SiO2<KCl
C.酸性:HClO4>H3PO4>H2SO4>H2SiO3
D.粒子半径:K+>Na+>Mg2+>Al3+
D
【解析】
试题分析:A、元素的非金属性越强,氢化物的稳定性越强,故稳定性:H2O>NH3>PH3>SiH4 ,错误;B、二氧化硅为原子晶体,氯化钾为离子晶体,故熔点:CO2<H2O<KCl<SiO2,错误;C、元素的非金属性越强,最高价氧化物水化物的酸性越强,故酸性:HClO4>H2SO4>H3PO4>H2SiO3,错误;D、根据微粒半径比较原则判断,粒子半径:K+>Na+>Mg2+>Al3+,正确。
考点:考查元素周期律。

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
X 、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是
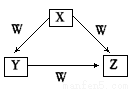
| X | Y | Z | W |
A | C | CO | CO2 | O2 |
B | Na | Na2O | Na2O2 | O2 |
C | AlCl3 | Al(OH)3 | NaAl(OH)4 | NaOH |
D | Fe | FeCl2 | FeCl3 | Cl2 |
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
选项 | 现象或事实 | 解 释 |
A | 用浸泡酸性高锰酸钾溶液的硅土延长果实的成熟 | 利用乙烯可以发生加成反应
|
B | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl反应生成氨气会降低肥效 |
C | SO2能使品红溶液褪色 | SO2具有还原性 |
D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含有Cu2+的溶液中置换出铜 |
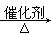 CH3CH2Br
CH3CH2Br
 CH2Cl2+2HCl
CH2Cl2+2HCl