题目内容
(每空2分,共12分)
PCl3与PCl5均是有机合成的重要中间体,两者存在以下相互转化关系:
PCl5(g)  PCl3(g) + Cl2(g) △H=a kJ·mol-1 在210℃时,将4mol PCl5气体充入
PCl3(g) + Cl2(g) △H=a kJ·mol-1 在210℃时,将4mol PCl5气体充入
2L真空密闭容器中发生上述反应,得到如下数据:
时间(s) | 0 | 20 | 40 | 60 |
n(PCl5) | 4 | 2.8 | 2 | 2 |
(1)已知上述反应在温度较高时才能自发进行,则a 0(填﹥、﹦、﹤);
(2)计算从20s至40s共20s的时间内,用PCl3表示的平均反应速率为 。210℃时该反应的平衡常数K值等于 。
(3)反应进行至60s后,将混合物的温度降低,重新达到平衡后氯气浓度将 (填“增大”、“减少”或“不变”)。
(4)欲增大该反应的K值,可采取的措施有(填序号)
A.降低温度 B.向混合气体中通入Cl2
C.使用高效催化剂 D.升高温度
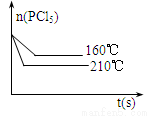
(5)如右图是210℃时容器中PCl5物质的量的变化曲线,请在该图中补画出该反应在160℃时PCl5物质的量的变化曲线。

(1) ﹥
(2)0.02mol·L-1·s-1。1mol·L-1(不带单位也给分)
(3)减少
(4)D
(5)
【解析】
试题分析:(1)PCl5(g)  PCl3(g) + Cl2(g) △S>0,且该反应在高温下自发,则△G=△H-T△S在高温下小于0,所以△H>0,该反应是吸热反应;
PCl3(g) + Cl2(g) △S>0,且该反应在高温下自发,则△G=△H-T△S在高温下小于0,所以△H>0,该反应是吸热反应;
(2)从20s至40s共20s的时间内,n(PCl5)减少2.8-2=0.8mol,所以PCl3的物质的量增加0.8mol,用PCl3表示的平均反应速率为0.8mol/2L/20s=0.02 mol·L-1·s-1;平衡时c(PCl5)=2mol/2L=1mol/L,PCl5的浓度减少4mol/2L-1mol/L=1mol/L,则平衡时c(PCl3)=c(Cl2)=1mol/L,所以平衡常数K= c(PCl3)×c(Cl2)/ c(PCl5)=1mol·L-1;
(3)该反应是吸热反应,温度降低,平衡逆向移动,所以再达平衡时氯气的浓度减少;
(4)平衡常数只与温度有关,温度高对正反应有利,平衡常数增大,所以欲增大该反应的K值,只能升高温度,答案选D;
(5)温度降低,反应速率减小,达到平衡的时间加长,同时平衡逆向移动,PCl5的物质的量增加,所以与210℃的图像相比,160℃的图像在210℃图像的上方,且后出现拐点,对应的图像见答案。
考点:考查对化学平衡常数、反应速率的计算,化学反应与能量的关系,化学平衡图像的描述

 名校课堂系列答案
名校课堂系列答案 CH3CH2Br
CH3CH2Br
 CH2Cl2+2HCl
CH2Cl2+2HCl