��Ŀ����
12����1��ʵ���ҿ���Ũ����Ͷ������̷�Ӧ�Ʊ�Cl2��MnO2+4HCl��Ũ�� $\frac{\underline{\;\;��\;\;}}{\;}$ MnCl2+Cl2��+2H2O
ȡ1.74g����������20mL 36.5% �����ᣨ�ܶ�Ϊ1.2g•mL-1����Ӧ�����ɵ������ڱ�״���µ����Ϊ0.448L�� ��Ӧ�����Һ�м���100mLijAgNO3��ҺʹCl-ǡ����ȫ��������AgNO3��Һ�����ʵ���Ũ��Ϊ2mol•L-1��
��2������480mL 0.1mol•L-1 HCl��Һ������������У���Ͳ���ձ�������������ͷ�ιܣ�����Ҫ�IJ���������500mL����ƿ��
����ʱ�������������������Һ��Ũ��ƫС����ac������ţ���
a���ձ���HCl��Һ��������ƿ��û��ϴ���ձ���ת��ϴ��Һ
b��ʵ���õ�����ƿϴ����δ������溬������ˮ
c�����ݺ�ҡ�ȣ�����Һ����ڿ̶��ߣ��ٵμ�����ˮ���̶���
d������ʱ���ӣ�
���� ��1��17.4g�������̺�36.5%Ũ����20mL���ܶ�Ϊ1.2g/mL����ַ�Ӧ�������������ʵ���Ϊ0.2mol��Ũ�������Ȼ������ʵ���=$\frac{20ml��1.2g/ml��36.5%}{36.5g/mol}$=0.24mol���������Ȼ��������MnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O�����ݶ������̼����������ʵ���Ϊ0.02mol�����Ա�״���£�VCl2=0.448L��������Ag++Cl-=AgCl��������Һ�е������ӵ����ʵ����ǣ�0.24mol-0.02mol��2=0.2mol��������������ʵ���Ϊ0.2mol���Ӷ�������ʵ���Ũ��c=$\frac{0.2}{100��1{0}^{-3}}$=2mol•L-1��
��2��������ɣ���ȱ�ٵIJ�������Ϊ500mL����ƿ��
a���ձ���HCl��Һ��������ƿ��û��ϴ���ձ���ת��ϴ��Һ�����������ʧ��Ũ��ƫС��
b��ʵ���õ�����ƿϴ����δ������溬������ˮ����Ũ����Ӱ�죻
c�����ݺ�ҡ�ȣ�����Һ����ڿ̶��ߣ��ٵμ�����ˮ���̶��ߣ��൱��ϡ����Һ��Ũ��ƫ�ͣ�
d������ʱ���ӣ��������ƫ��ˮ�����ˣ�Ũ��ƫ��
��� �⣺��1��17.4g�������̺�37%Ũ����200mL���ܶ�Ϊ1.19g/mL����ַ�Ӧ�������������ʵ���Ϊ0.2mol��Ũ�������Ȼ������ʵ���=$\frac{200ml��1.19g/ml��37%}{36.5g/mol}$=2.4mol���������Ȼ��������MnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O�����ݶ������̼����������ʵ���Ϊ0.2mol�����Ա�״���£�VCl2=4.48L������Ag++Cl-=AgCl��������Һ�е������ӵ����ʵ����ǣ�0.24mol-0.02mol��2=0.2mol��������������ʵ���Ϊ0.2mol���Ӷ�������ʵ���Ũ��c=$\frac{0.2}{100��1{0}^{-3}}$=2mol•L-1��
�ʴ�Ϊ��4.48L��2mol•L-1��
��2��������ɣ���ȱ�ٵIJ�������Ϊ500mL����ƿ��
a���ձ���HCl��Һ��������ƿ��û��ϴ���ձ���ת��ϴ��Һ�����������ʧ��Ũ��ƫС����a��ȷ��
b��ʵ���õ�����ƿϴ����δ������溬������ˮ����Ũ����Ӱ�죬��b����
c�����ݺ�ҡ�ȣ�����Һ����ڿ̶��ߣ��ٵμ�����ˮ���̶��ߣ��൱��ϡ����Һ��Ũ��ƫ�ͣ���c��ȷ��
d������ʱ���ӣ��������ƫ��ˮ�����ˣ�Ũ��ƫ��d����
�ʴ�Ϊ��ac��
���� ���⿼�黯ѧ����ʽ�йؼ��㣬�Ƚϻ�����ע��Ի���֪ʶ���������գ�

| A�� | ��Ԫ�ص���������ϼ۸����������� | |
| B�� | ����Ԫ�ض��������ϼۺ����ϼۣ����ǵľ���ֵ֮�͵���8 | |
| C�� | �ǽ���Ԫ�صĸ����ϼۣ�����ԭ�������ﵽ8�������ȶ��ṹ����õ��ĵ����� | |
| D�� | ��Ԫ��ԭ�ӵ���������������������� |
| ���ữѧʽ | CH3COOH | HCN | H2CO3 |
| ����ƽ�ⳣ����25�棩 | 1.8��10-5 | 4.9��10-10 | Ka1=4.3��10-7 Ka2=5.6��10-11 |
| A�� | �����ʵ���Ũ�ȵĸ���Һ pH ��ϵΪ��pH �� NaCN����pH��Na2CO3����pH�� CH3COONa�� | |
| B�� | Ũ�Ⱦ�Ϊ0.2mol/L NaHCO3�� Na2CO3��Һ�У����ڵ����������ͬ | |
| C�� | 0.4 mol•L-1HCN ��Һ�� 0.2 mol•L-1NaOH ��Һ�������Ϻ�������Һ�У�c��Na+����c��OH-����c��H+�� | |
| D�� | 25��ʱ��pH=4��Ũ�Ⱦ�Ϊ0.1 mol•L-1�� CH3COOH��CH3COONa�����Һ�У�c��Na+��+c��H+����c��CH3COO-��+c��CH3COOH�� |
| A�� | ������Һ��ˮ�����c��OH-��=1.0��10-10mol•L-1 | |
| B�� | ������Һ�е�c��Cu2+��=1.0��10-5mol•L-1 | |
| C�� | ��������Һ�еμ�Na2S��Һ���к�ɫ�������� | |
| D�� | ��ȥ��ҵ��ˮ�е�Cu2+��������FeS�������� |
 һ���¶��£���һ�������ı������ˮϡ�����У���Һ�ĵ��������仯��ͼ��ʾ�������й�a��b��c�����˵������ȷ���ǣ�������
һ���¶��£���һ�������ı������ˮϡ�����У���Һ�ĵ��������仯��ͼ��ʾ�������й�a��b��c�����˵������ȷ���ǣ�������| A�� | ����ĵ���̶��ɴ�С��˳��b��c��a | |
| B�� | ��Һ��pH�ɴ�С��˳��a��c��b | |
| C�� | ��ʪ���pH��ֽ����������Һ��pH�����������ƫ�� | |
| D�� | ��Һ��$\frac{{c��C{H_3}COOH��}}{{c��C{H_3}CO{O^-}��}}$����ֵ���� |
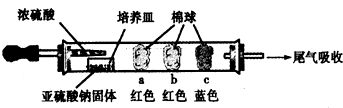
������ʵ�飺��ͼ��ʾ����Ũ�������װ��Na2SO3�����������һ��ʱ���a��b��c��������仯���±�������д���еĿհף�
| ���� | �����ϵμӵ��Լ� | ʵ������ | ���ͺͽ��� |
| a | Ʒ����Һ | �����ף��Ⱥ��ָֻ���ɫ | SO2����Ư���ԣ���Ϊ��ʱ��Ư�� |
| b | ����̪��NaOH��Һ | �����Ϊ��ɫ | ���ӷ���ʽ��2OH��+SO2 =SO32��+H2O��OH��+SO2=HSO3�� |
| c | �����۵ĵ�ˮ | �����Ϊ��ɫ | ��������л�ԭ�� ��ѡ������ԡ���ԭ�ԡ��� |
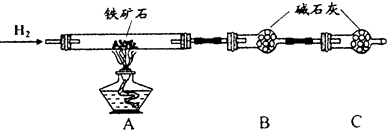
ʵ��һ������ʯ�к������IJⶨ
��1������ͼ��װ�������г�������ʡ�ԣ������װ�õ������ԣ�
��2����10.0g����ʯ����Ӳ�ʲ������У�
��3������˵����ܿڴ����ϵػ���ͨ��H2����Cװ�ó��ڴ�H2�鴿��ȼA���ƾ��ƣ�
��4����ַ�Ӧ�����ƾ��ƣ��ٳ���ͨ����������ȫ��ȴ��
��5����÷�Ӧ��װ��B����2.70g��������ʯ��������������Ϊ24%��
ʵ���������ʯ�к������IJⶨ
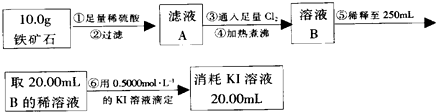
��1������ں͢��ж�Ҫ�õ��IJ����������ձ�����������
��2�������йز���IJ�����˵������ȷ����bc��
a���ζ���������ˮϴ�Ӻ����ô�װҺ��ϴ
b����ƿ��Ҫ�ô���Һ��ϴ
c����Ϊ��ˮΪ��ɫ�����Եζ������в����ָʾ��
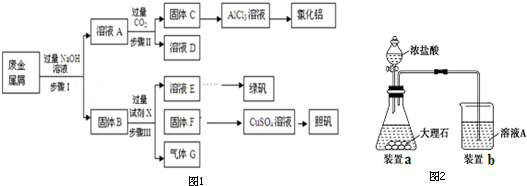
ʵ����ۣ������������������ɣ���ʵ��һ�����ó�������ʯ������������Ļ�ѧʽΪFe5O6��
| A�� | ҽ�þƾ���Ũ��ͨ��Ϊ95% | |
| B�� | ���ۡ���ά�غ���֬��������Ȼ�߷��ӻ����� | |
| C�� | ��ˮ�ӵĸ���բ����ֱ����������������Է�բ�Ÿ�ʴ | |
| D�� | ��������Ƭ��ά����Cͬʱ���ã�����ǿ����ȱ����ƶѪ��Ч�� |
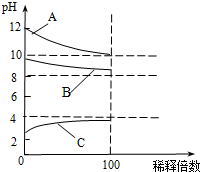 ���г���ʱŨ����ͬ�����ֵ������Һ����CH3COOH ��Na2CO3 ��HNO3��CH3COONa ��NaOH
���г���ʱŨ����ͬ�����ֵ������Һ����CH3COOH ��Na2CO3 ��HNO3��CH3COONa ��NaOH