题目内容
18.在一定条件下,RO${\;}_{3}^{n-}$和I-可以发生反应,离子方程式为RO${\;}_{3}^{n-}$+6I-+6H+═R-+3I2+3H2O根据计算回答:
(2)RO${\;}_{3}^{n-}$中n值为1;
(2)RO${\;}_{3}^{n-}$中元素R的化合价为+5.
分析 根据电荷守恒规律,先计算出n值,然后再根据化合价规律计算出R的正化合价,再由R的正化合价去确定最外层的电子数.
解答 解:(1)根据离子方程式为RO3n-+6I-+6H+═R-+3I2+3H2O,结合电荷守恒规律,则-n+6×(-1)+6×(+1)=-1,解得n=1,故答案为:1;
(2)因为n=1,设RO3-中R元素的化合价为x,则x+3×(-2)=-1,解得x=+5,故答案为:+5.
点评 本题根据电荷守恒规律,化合价规律计算化合价,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列变化一定有旧的化学键断裂,新的化学键形成的是( )
| A. | 将氯化钠固体加热到熔融状态产生Na+和Cl- | |
| B. | 将碘单质加热升华 | |
| C. | 将氯化氢气体通入水产生H+和Cl- | |
| D. | 在放电条件下氧气转化为臭氧 |
9.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目为NA | |
| B. | 1 L 0.1 mol•L-1的氨水中有0.1NA个NH4+ | |
| C. | 常温常压下,8 g O2含有4 NA个电子 | |
| D. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA |
1.柠檬烯是一种常用香料,其结构简式如图.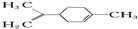 有关柠檬烯的分析正确的是( )
有关柠檬烯的分析正确的是( )
 有关柠檬烯的分析正确的是( )
有关柠檬烯的分析正确的是( )| A. | 它的一氯代物有6种 | |
| B. | 它和丁基苯( 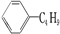 )互为同分异构体 )互为同分异构体 | |
| C. | 它的分子中所有的碳原子一定在同一平面上 | |
| D. | 一定条件下,它分别可以发生加成、取代、氧化、还原等反应 |
8.下列装置能够组成原电池且正极质量增加的是( )
| A. | 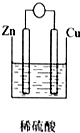 | B. | 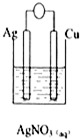 | C. | 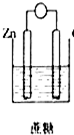 | D. | 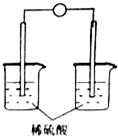 |
6. 如图所示在密封容器中,一部分装入2.3g金属钠,另一部分装入HgO,同时加热两部分,若加热后容器内的空气成分未变,那么装入容器中的HgO是( )
如图所示在密封容器中,一部分装入2.3g金属钠,另一部分装入HgO,同时加热两部分,若加热后容器内的空气成分未变,那么装入容器中的HgO是( )
 如图所示在密封容器中,一部分装入2.3g金属钠,另一部分装入HgO,同时加热两部分,若加热后容器内的空气成分未变,那么装入容器中的HgO是( )
如图所示在密封容器中,一部分装入2.3g金属钠,另一部分装入HgO,同时加热两部分,若加热后容器内的空气成分未变,那么装入容器中的HgO是( )| A. | 21.6 g | B. | 20.0g | C. | 1.6 g | D. | 10.8 g |
 .
.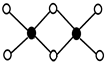 硼及其化合物在工业上有许多用途.工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5•H2O和Fe3O4.
硼及其化合物在工业上有许多用途.工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5•H2O和Fe3O4.