题目内容
8.下列装置能够组成原电池且正极质量增加的是( )| A. | 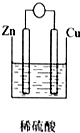 | B. | 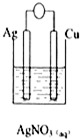 | C. | 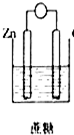 | D. | 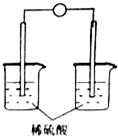 |
分析 构成原电池需具备以下条件:两个活性不同的电极;电解质溶液;形成闭合回路;存在能自动发生的氧化还原反应,且为放热反应,以此来解答.
解答 解:A、可以构成原电池,但正极是氢离子放电生成氢气,正极质量不变,故A不符合;
B、符合构成原电池,正极银上银离子放电生成单质银,质量增加,故B符合;
C、蔗糖非电解质,不能构成原电池,故C 不符合;
D、没有形成闭合回路,不能构成原电池,故D不符合;
故选:B.
点评 本题考查了原电池原理的分析应用,该题是高考中的常见考点,属于基础性试题的考查,难度不大.明确原电池的工作原理、构成条件是答题的关键.

练习册系列答案
相关题目
1. 三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述不正确的是( )
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述不正确的是( )
 三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述不正确的是( )
三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室.下列叙述不正确的是( )| A. | 当电路中通过4mol电子的电量时,生成有标准状况下的O2为22.4L | |
| B. | 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品 | |
| C. | 正极区反应为2H2O-4e-═O2+4H+,正极区溶液pH降低 | |
| D. | 通电后中间隔室的SO42-离子向负极区迁移,负极区溶液pH增大 |
3.下列物质中,含有Cl-的是( )
①盐酸 ②氯化钠溶液 ③氯化钠固体 ④次氯酸 ⑤氯化氢气体⑥氯仿.
①盐酸 ②氯化钠溶液 ③氯化钠固体 ④次氯酸 ⑤氯化氢气体⑥氯仿.
| A. | ①②⑥ | B. | ①②③ | C. | ③④⑥ | D. | ②④⑤ |
17.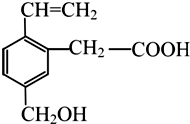 某有机物的结构如图所示,这种有机物具有的性质是( )
某有机物的结构如图所示,这种有机物具有的性质是( )
①可以与氢气发生加成反应;
②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应;
④能发生酯化反应;
⑤能发生加聚反应.
 某有机物的结构如图所示,这种有机物具有的性质是( )
某有机物的结构如图所示,这种有机物具有的性质是( )①可以与氢气发生加成反应;
②能使酸性KMnO4溶液褪色;
③能跟NaOH溶液反应;
④能发生酯化反应;
⑤能发生加聚反应.
| A. | 只有①④ | B. | 只有①④⑤ | C. | ①②③④ | D. | 全部 |
18.下列颜色变化与氧化还原反应无关的是( )
| A. | 将乙醛加入新制氢氧化铜中加热,出现砖红色沉淀 | |
| B. | 将乙醇滴入酸性重铬酸钾溶液中,溶液由橙色变为绿色 | |
| C. | 将二氧化硫通入滴有酚酞的氢氧化钠溶液中,溶液红色褪去 | |
| D. | 新制氯水敞口久置,颜色褪去 |


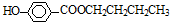 )可用作防腐剂,对酵母菌和霉菌有很强的抑制作用,工业上常用对羟基苯甲酸与丁醇在浓硫酸催化下进行酯化反应而制得.以下是某课题组开发的从廉价、易得的化工原料出发制备对羟基苯甲酸丁酯的合成路线:
)可用作防腐剂,对酵母菌和霉菌有很强的抑制作用,工业上常用对羟基苯甲酸与丁醇在浓硫酸催化下进行酯化反应而制得.以下是某课题组开发的从廉价、易得的化工原料出发制备对羟基苯甲酸丁酯的合成路线: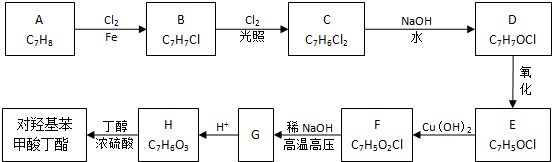
 +2Cu(OH)2 $\stackrel{△}{→}$
+2Cu(OH)2 $\stackrel{△}{→}$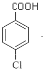 +Cu2O↓+2H2O;
+Cu2O↓+2H2O;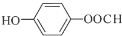 ,其核磁共振氢谱中不同化学环境的氢的峰面积比为1:2:2:1,它与足量NaOH溶液反应的方程式为
,其核磁共振氢谱中不同化学环境的氢的峰面积比为1:2:2:1,它与足量NaOH溶液反应的方程式为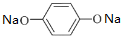 +HCOONa+2H2O.
+HCOONa+2H2O.