题目内容
5.下列有关说法中正确的是( )| A. | 离子化合物熔沸点较高、共价化合物熔沸点较低 | |
| B. | 全部由非金属元素组成的化合物不一定是共价化合物 | |
| C. | 离子半径:Na+>Mg2+>Al3+>F- | |
| D. | 熔点:金刚石>NaCl>CO2 |
分析 A、共价化合物包括分子晶体和原子晶体;
B、铵盐为离子化合物;
C、当电子层数相同时,核电荷数越大,半径越小;
D、物质的熔点的一般顺序为:原子晶体>离子晶体>分子晶体.
解答 解:A、共价化合物包括分子晶体和原子晶体,而物质的熔点的一般顺序为:原子晶体>离子晶体>分子晶体,故离子化合物的熔点不一定比共价化合物的高,故A错误;
B、铵盐全部由非金属元素构成,而铵盐为离子化合物,即由非金属元素构成的化合物不一定为共价化合物,故B正确;
C、当电子层数相同时,核电荷数越大,半径越小,故半径大小顺序为:F->Na+>Mg2+>Al3+,故C错误;
D、物质的熔点的一般顺序为:原子晶体>离子晶体>分子晶体,而金刚石为原子晶体,氯化钠为离子晶体,二氧化碳为分子晶体,故熔点顺序为:金刚石>氯化钠>二氧化碳,故D正确.
故选BD.
点评 本题考查化学键,熟悉常见物质中的化学键及物质的性质是解答的关键,并学会利用举例的方法来解答.

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
16.下列分散系能产生丁达尔效应的是( )
| A. | 稀豆浆 | B. | 稀硫酸 | C. | 氢氧化钠溶液 | D. | 食盐水 |
13.加热装有1mol NH3气体的定容密闭容器,在T1℃时,2NH3(g)?N2(g)+3H2 △H>0.
反应达到平衡时.N2的物质的量分数为X1;若起始时,在该容器中加热2mol NH3,在T2℃达到平衡时.N2的物质的量分数为x2,则下列关系一定正确的是( )
反应达到平衡时.N2的物质的量分数为X1;若起始时,在该容器中加热2mol NH3,在T2℃达到平衡时.N2的物质的量分数为x2,则下列关系一定正确的是( )
| A. | 若T1=T2,则x1>x2 | B. | 若T1=T2,则x1<x2 | C. | 若T1<T2,则x1=x2 | D. | 若T1<T2,则x1<x2 |
20.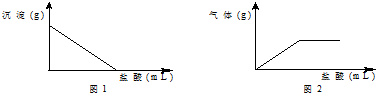 有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.下列根据实验事实得出的结论正确的是( )
有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.下列根据实验事实得出的结论正确的是( )
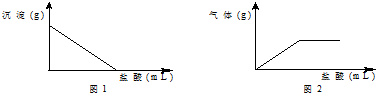 有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.下列根据实验事实得出的结论正确的是( )
有一包白色固体,可能含有Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种.下列根据实验事实得出的结论正确的是( )| A. | 取样溶于水,有白色沉淀产生,说明原白色固体中一定有Na2SO4和BaCl2 | |
| B. | 取样溶于水,静置后测得上层清液的pH>7,说明原白色固体中一定有NaOH | |
| C. | 取样溶于水,有白色沉淀产生,过滤后向沉淀中滴加盐酸,沉淀的量与加入盐酸体积的关系如图1所示,则原白色固体中无Na2SO4 | |
| D. | 取样溶于水,有白色沉淀产生,过滤后向沉淀中滴加盐酸,产生气体的量与加入盐酸体积的关系如图2所示,则该白色固体中无NaOH |
17.地壳中铜元素的含量远比铁元素少,但历史上金属铜的使用比铁要早得多,如铜钱曾经是历史上广泛使用的货币,用铜而不用铁铸钱币的理由是:( )
①铜的化学性质比较稳定,不易腐蚀.②铜的熔点较低,易冶炼③铜的硬度较小,易加工.
①铜的化学性质比较稳定,不易腐蚀.②铜的熔点较低,易冶炼③铜的硬度较小,易加工.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
14.下列关于物质或离子检验的叙述正确的是( )
| A. | 向某溶液中加入BaCl2溶液,出现白色沉淀,再加稀硝酸溶液,若沉淀不溶解,则该溶液中肯定有SO42- | |
| B. | 灼烧某白色粉末,火焰呈黄色,则证明原粉末中肯定有Na+,无K+ | |
| C. | 向某溶液中滴加AgNO3溶液后,出现白色沉淀,再加稀盐酸,若沉淀不溶解,则证明溶液中肯定有Cl- | |
| D. | 在某盐溶液中加入氢氧化钠浓溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝,则该溶液中肯定有NH4+ |
15.阿司匹林的结构简式如图,把阿司匹林放在足量的氢氧化钠溶液中煮沸,能发生反应的化学键是( )


| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |