题目内容
1.已知在标况下的四种气体①6.72LCH4 ②3.01×1023个HCl分子 ③13.6克H2S④0.2molNH3用相应的序号填写下列空白:(1)体积最大的是②;
(2)原子数最多的是①;
(3)质量最小的是④;
(4)含氢原子数最少的是②.
分析 标况下Vm=22.4L/mol,根据n=$\frac{V}{{V}_{m}}$=$\frac{N}{{N}_{A}}$=$\frac{m}{M}$分别计算出各物质的物质的量,然后分别计算出标准状况下的气体体积、含有原子的物质的量、含有氢原子的物质的量及质量,据此进行计算.
解答 解:①6.72LCH4中:n(CH4)=$\frac{6.72L}{22.4L/mol}$=0.3mol,m(CH4)=0.3mol×16g/mol=4.8g,含有原子数的物质的量为:0.3mol×5=1.5mol,N(H)=4N(CH4)=1.2NH3;
②3.01×1023个HCl分子中:n(HCl)=$\frac{3.01×1{0}^{23}}{6.02×1{0}^{23}}$mol=0.5mol,V(HCl)=0.5mol×22.4L/mol=11.2L,含有原子的物质的量为0.5mol×2=1mol;
③13.6克H2S 中:n(H2S)=$\frac{13.6g}{34g/mol}$=0.4mol,V(H2S)=0.4mol×22.4L/mol=8.96L,含有原子的物质的量为:0.4mol×3=1.2mol,N(H)=2N(H2S)=0.8NA;
④0.2molNH3中:m(NH3)=0.2mol×17g/mol=3.4g,V(NH3)=0.2mol×22.4L/mol=4.48L,含有原子的物质的量为:0.2mol×4=0.8mol,N(H)=3N(NH3)=0.6NH3.
(1)根据分析可知,气体体积最大的是②,
故答案为:②;
(2)根据N=nNA可知,气体的物质的量越大,含有原子数越大,则含有原子数最多的为①,
故答案为:①;
(3)质量最小的是④,
故答案为:④;
(4)含氢原子数最少的是②,
故答案为:②.
点评 本题考查物质的量的相关计算,题目难度不大,明确物质的量与摩尔质量、阿伏伽德罗常数、气体摩尔体积之间的关系即可解答,试题培养了学生的分析能力及化学计算能力.

| A. | 无色溶液:Ca2+、H+、Cl-、HSO3- | |
| B. | 能使pH试纸呈红色的溶液:Na+、NO3-、I-、AlO2- | |
| C. | FeCl3溶液:K+、Na+、Fe2+、S2- | |
| D. | $\frac{{K}_{W}}{c({H}^{+})}$=0.1mol/L的溶液:Na+、K+、SiO32-、NO3- |
①3Cl2+6KOH═5KCl+KClO3+3H2O ②3NO2+H2O═2HNO3+NO
③SnCl4+2H2O═SnO2+4HCl ④NaOH+HCl═H2O+NaCl.
| A. | ①② | B. | ②③ | C. | ①③ | D. | ③④ |
| A. | Na+、Al3+、SO42-、NO3- | B. | K+、Na+、SO42-、Ba2+ | ||
| C. | K+、MnO4-、NH4+、Cl- | D. | Cu2+、K+、HCO3-、NO3- |
| A. | SO2可用于杀菌、消毒 | B. | HF可用于雕刻玻璃 | ||
| C. | NH3可用于制硝酸 | D. | SiO2可用于制太阳能电池 |
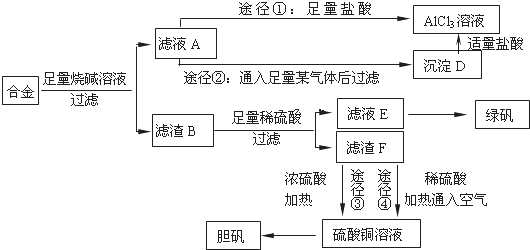
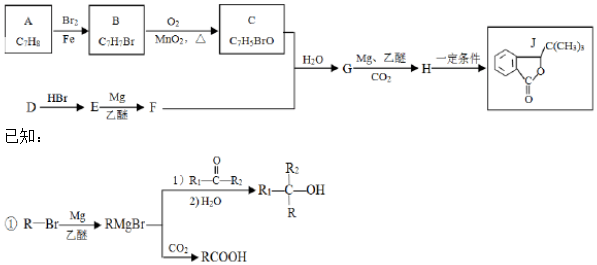
 .
. (写结构简式).
(写结构简式).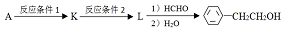
 .
.