题目内容
20.下列各图所示的实验原理、方法、装置和操作正确的是( )| A. | 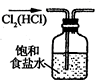 除去Cl2中HCl | B. | 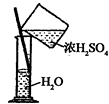 稀释浓H2SO4 | C. | 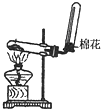 制取氧气 | D. | 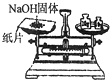 称取NaOH |
分析 A.氯气在饱和食盐水中的溶解度比较小;
B.量筒不能稀释溶液;
C.氧气密度比空气大;
D.称量氢氧化钠时要放置在小烧杯中.
解答 解:A.氯气在饱和食盐水中的溶解度比较小,可除掉氯化氢,故A正确;
B.量筒只能用来量取溶液,不能稀释或溶解药品,故B错误;
C.氧气密度比空气大,应用向上排空气法收集,故C错误;
D.氢氧化钠具有强腐蚀性,能潮解,所以称量氢氧化钠时要放置在小烧杯中,故D错误;
故选A.
点评 本题考查了化学实验评价,明确实验原理是解本题关键,熟悉常见仪器的作用、实验基本操作规范、常见气体的制取和收集元素等知识点即可解答,题目难度不大.

练习册系列答案
相关题目
15.下列有关实验原理、现象、结论等均正确的是( )
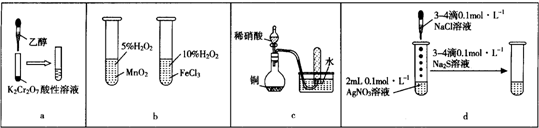

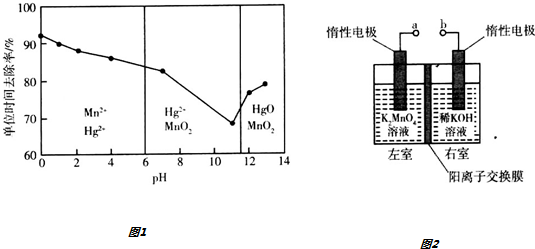
| A. | a图示装置,滴加乙醇试管中橙色溶液变为绿色,乙醇发生消去反应生成乙酸 | |
| B. | b图示装置,右边试管中产生气泡迅速,说明氯化铁的催化效果比二氧化锰好 | |
| C. | c图示装置,根据试管中收集到无色气体,验证铜与稀硝酸的反应产物是NO | |
| D. | d图示装置,试管中先有白色沉淀、后有黑色沉淀,不能验证AgCl的溶解度大于Ag2S |
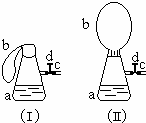 如图(Ⅰ)中锥形瓶a内放入43.8g10%的稀盐酸,b是未充气的气球,里边放有4g碳酸钙粉末,将它紧紧套在瓶a口上,胶管c套在瓶的侧口,并用弹簧夹d夹紧(瓶口和侧口都不漏气).将图Ⅰ的装置在托盘天平上称量,质量为W1克.根据实验现象填写下列空白:
如图(Ⅰ)中锥形瓶a内放入43.8g10%的稀盐酸,b是未充气的气球,里边放有4g碳酸钙粉末,将它紧紧套在瓶a口上,胶管c套在瓶的侧口,并用弹簧夹d夹紧(瓶口和侧口都不漏气).将图Ⅰ的装置在托盘天平上称量,质量为W1克.根据实验现象填写下列空白: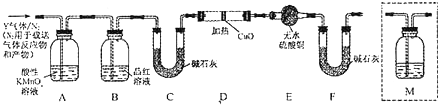
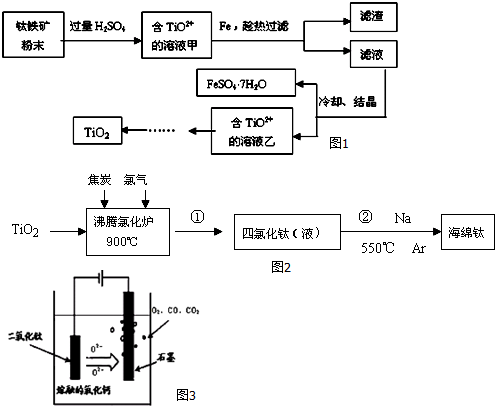
 ,P元素属于ds区元素.
,P元素属于ds区元素.