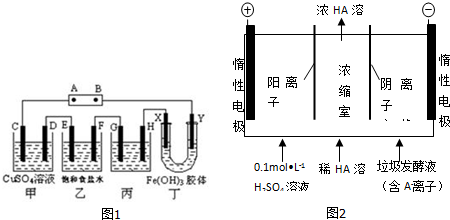
题目内容
9.I.碱性锌锰干电池的总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2.该电池中,负极材料是Zn,正极反应式为MnO2+H2O+e-═MnOOH+OH-.Ⅱ.以废旧锌锰干电池处理得到的混合物为原料制备锰锌铁氧体的主要流程如图所示.
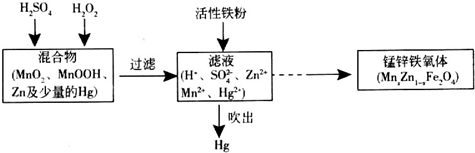
请回答下列问题:
(1)MnxZn1-xFe2O4中铁元素化合价为+3,则锰元素的化合价为+2.
(2)活性铁粉除汞时,铁粉的作用是还原剂(填“氧化剂”或“还原剂”).
(3)除汞是以氮气为载气吹入滤液中,带出汞蒸气经KMnO4溶液进行吸收而实现的.在恒温下不同pH时,KMnO4溶液对Hg的单位时间去除率及主要产物如图1所示.
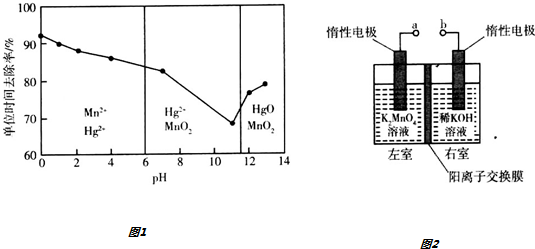
①写出pH=2时KMnO4溶液吸收汞蒸气的离子方程式5Hg+2MnO4-+16H+═2Mn2++5Hg2++8H2O.
②在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4;溶液的氧化性增强外,还可能是Mn2+对反应起催化作用,单位时间内去除率高.
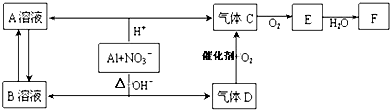
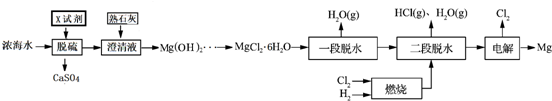
(4)用惰性电极电解K2MnO4溶液制备KMnO4的装置如图2所示.
①a应接直流电源的正(填“正”或“负”)极.
②已知25℃,两室溶液的体积均为100mL,电解一段时间后,右室溶液的pH由10变为14,则理论上可制得0.1mol KMnO4 (忽略溶液的体积和温度变化).
分析 I.负极发生氧化反应,电极反应式为Zn+2OH--2e-═Zn(OH)2,总反应式减去负极反应式可得正极反应式;
Ⅱ.(1)根据化合价规则判断锰元素的化合价;
(2)由流程可知活性铁粉除汞时,Hg2+被还原为Hg;
(3)①根据题给图象知pH=2时KMnO4溶液吸收汞蒸气生成Mn2+和Hg2+;
②不考虑酸性条件下氧化性增强因素,酸性条件下有Mn2+生成,可能是Mn2+具有催化作用;
(4)①左室K2MnO4发生氧化反应生成KMnO4,故左侧电极为电解池的阳极;
②电解过程中阳极反应为MnO42--e-═MnO4-,阴极反应为2H2O+2e-═H2↑+2OH-,根据右室pH变化计算生成OH-的物质的量为0.1mol,再结合电子转移守恒计算.
解答 解:I.碱性锌锰干电池的总反应为Zn+2MnO2+2H2O═2MnOOH+Zn(OH)2,原电池中负极发生氧化反应,负极材料是Zn,电极反应式为:Zn+2OH--2e-═Zn(OH)2,总反应式减去负极反应式可得正极反应式,则正极反应式为:MnO2+H2O+e-═MnOOH+OH-,
故答案为:Zn;MnO2+H2O+e-═MnOOH+OH-;
Ⅱ.(1)MnxZn1-xFe2O4中铁元素化合价为+3,根据化合价代数和为0,可知锰元素的化合价为+2价,
故答案为:+2;
(2)由流程知活性铁粉除汞时,Hg2+被还原为Hg,铁粉的作用是还原剂,
故答案为:还原剂;
(3)①根据题给图象知pH=2时KMnO4溶液吸收汞蒸气生成Mn2+和Hg2+,反应的离子方程式为:5Hg+2MnO4-+16H+═2Mn2++5Hg2++8H2O,
故答案为:5Hg+2MnO4-+16H+═2Mn2++5Hg2++8H2O;
②在强酸性环境中汞的单位时间去除率高,其原因除氢离子浓度增大使KMnO4溶液的氧化性增强外,还可能是生成的Mn2+对反应起催化作用,单位时间内去除率高,
故答案为:Mn2+对反应起催化作用,单位时间内去除率高;
(4)①左室K2MnO4发生氧化反应生成KMnO4,故左侧电极为电解池的阳极,a应接直流电源的正极,
故答案为:正;
②电解过程中阳极反应为MnO42--e-═MnO4-,阴极反应为2H2O+2e-═H2↑+2OH-,已知25℃,两室溶液的体积均为100mL,电解一段时间后,右室溶液的pH由10变为14,电解后氢氧根离子浓度为1mol/L,则生成OH-的物质的量约是为0.1L×1mol/L=0.1mol,由电子转移守恒可知,理论上可制得0.1mol KMnO4,
故答案为:0.1mol.
点评 本题考查化学工艺流程、读图获取信息能力、电化学等,侧重考查学生对知识的迁移运用,难度中等.

 阅读快车系列答案
阅读快车系列答案| 离子 | Na+ | Mg2+ | Cl- | SO42- |
| 浓度/(g•L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
请回答下列问题
(1)浓海水主要含有的四种离子中质量浓度最小的是Mg2+.在上述流程中,可以循环使用的物质是Cl2、HCl.
(2)在该工艺过程中,X试剂的化学式为CaCl2.
(3)“一段脱水”目的是制备MgCl2•2H2O;“二段脱水”的目的是制备电解原料.若将MgCl2•6H2O直接加热脱水,则会生成Mg(OH)Cl.若电解原料中含有Mg(OH)Cl,电解时Mg(OH)Cl与阴极产生的Mg反应,使阴极表面产生MgO钝化膜,降低电解效率.生成MgO的化学方程式为2Mg(OH)Cl+Mg=MgCl2+2MgO+H2↑.
(4)若制得Mg(OH)2的过程中浓海水的利用率为80%,由Mg(OH)2至“二段脱水”制得电解原料的过程中镁元素的利用率为90%,则1m3浓海水可得“二段脱水”后的电解原料质量为84672g.
(5)以LiCl-KCl共熔盐为电解质的Mg-V2O5电池是战术导弹的常用电源,该电池的总反应为:Mg+V2O5+2LiCl═MgCl2+V2O4•Li2O 该电池的正极反应式为V2O5+2Li++2e-=V2O4•Li2O.
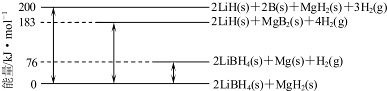
(6)Mg合金是重要的储氢材料.2LiBH4/MgH2体系放氢焓变示意图如下,则:
Mg(s)+2B(s)═MgB2(s)△H=-93 kJ•mol-1.
| A. | 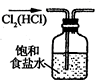 除去Cl2中HCl | B. | 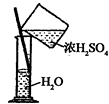 稀释浓H2SO4 | C. | 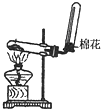 制取氧气 | D. | 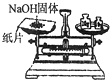 称取NaOH |
| A. | $\frac{125a}{288V}$mol•L-1 | B. | $\frac{125a}{72V}$mol•L-1 | ||
| C. | $\frac{a}{2304V}$mol•L-1 | D. | 以上答案均不正确 |
| A. | Fe | B. | P | C. | Mg | D. | Cu |
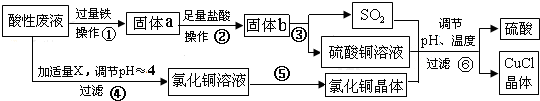

 +2H2C=CH2$\stackrel{一定条件}{→}$
+2H2C=CH2$\stackrel{一定条件}{→}$
 +2H2C=CH2$\stackrel{一定条件}{→}$
+2H2C=CH2$\stackrel{一定条件}{→}$
 .
. .
.