题目内容
 参考下列图表和有关要求回答问题:
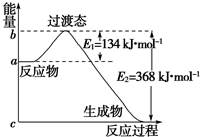
参考下列图表和有关要求回答问题:(1)如图是1mol NO2(g)和1mol CO(g)反应生成CO2和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJ?mol-1
②CH3OH(g)+
| 1 |
| 2 |
又知③H2O(g)═H2O(l)△H=-44kJ?mol-1 则甲醇燃烧生成液态水的热化学方程式为
考点:反应热和焓变,用盖斯定律进行有关反应热的计算
专题:化学反应中的能量变化
分析:(1)加入催化剂能降低反应所需的活化能,但是不改变反应物的总能量和生成物的总能量,由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368-134=234kJ,根据热化学方程式书写原则进行书写;
(2)依据热化学方程式,利用盖斯定律进行计算;
(2)依据热化学方程式,利用盖斯定律进行计算;
解答:
解:(1)加入催化剂能降低反应所需的活化能,则E1和E2都减小,催化剂不能改变反应物的总能量和生成物的总能量之差,即反应热不改变,所以催化剂对反应热无影响,由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368-134=234kJ,反应热化学方程式为NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ?mol-1,
故答案为:减小;不变;NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ?mol-1;
(2)利用盖斯定律进行计算,
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ?mol-1
②CH3OH(g)+
O2(g)=CO2(g)+2H2(g)△H=-192.9kJ?mol-1
又知 ③H2O(g)=H2O(l)△H=-44kJ/mol
依据盖斯定律计算(②×3-①×2+③×2)得到CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H=3×(-192.9 kJ?mol-1)-2×49.0 kJ?mol-1+(-44 kJ?mol-1)×2=-764.7 KJ/mol;
故答案为:CH3OH(l)+
O2(g)=CO2(g)+2H2O(l)△H=-764.7 KJ/mol;
故答案为:减小;不变;NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ?mol-1;
(2)利用盖斯定律进行计算,
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+49.0kJ?mol-1
②CH3OH(g)+
| 1 |
| 2 |
又知 ③H2O(g)=H2O(l)△H=-44kJ/mol
依据盖斯定律计算(②×3-①×2+③×2)得到CH3OH(l)+
| 3 |
| 2 |
故答案为:CH3OH(l)+
| 3 |
| 2 |
点评:本题考查较为综合,题目难度中等,本题注意热化学方程式的书写方法和计算应用,注意焓变计算和物质聚集状态的标注,学习中要准确把握

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
在氢气与氧气燃烧的过程中,破坏1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氧气中的化学键消耗的能量为Q2kJ,形成1mol水中的化学键释放的能量为Q3kJ.下列关系式中,正确的是( )
| A、Q1+Q2<Q3 |
| B、Q1+Q2>2Q3 |
| C、2Q1+Q2>2Q3 |
| D、2Q1+Q2<2Q3 |
下列叙述正确的是(NA为阿伏伽德罗常数)( )
| A、标况下,22.4L苯的分子数为NA |
| B、10.0mL 18mol/L的浓硫酸中氢离子数为0.36NA |
| C、6.4gS6与S8的混合物中所含S原子数一定为0.2NA |
| D、标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2NA |
要求设计实验证明某种盐的水解是吸热的,下列回答正确的是( )
| A、将硝酸铵晶体溶于水,若水温下降,说明硝酸铵水解是吸热的 |
| B、在盐酸中加入相同浓度的氨水,若混合液温度下降,说明盐类水解是吸热的 |
| C、在醋酸钠溶液中加入醋酸钠晶体,若溶液温度下降,说明盐类水解是吸热的 |
| D、在醋酸钠溶液中滴入酚酞试液,加热后若红色加深,说明盐类水解是吸热的 |
对于反应mA+nB═pC,下列说法正确的是( )
| A、某温度时,化学反应速率无论用A、B、C何种物质表示,其数值是相同的 |
| B、其他条件不变,增大压强,反应速率加快 |
| C、若增加或减小B的物质的量,则反应速率一定会发生明显的变化 |
| D、其他条件不变,升高温度,反应速率加快 |
下列小实验设计肯定合理的是( )
| A、用AgNO3鉴别工业盐(亚硝酸钠)和食盐二种溶液 |
| B、海带中碘元素提取时氧化滤液中的I-时应加入过量氯水 |
| C、将3-4个火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液、稀硝酸和NaNO2溶液,若出现白色沉淀,说明含有氯元素 |
| D、溶质的溶解度越大,溶液的浓度越高,溶剂的蒸发速度越快,溶液的冷却速度越快,析出的晶体就越细小 |
某离子化合物的晶胞如图所示立体结构,晶胞是整个晶体中最基本的重复单位.小黑球表示阳离子,小白球表示阴离子,该离子化合物中,阴、阳离子个数比是( )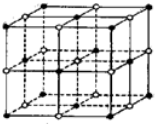

| A、1:8 | B、1:4 |
| C、1:2 | D、1:1 |
 实验室欲配制0.05mol?L-1的NaOH溶液500mL,有以下仪器:
实验室欲配制0.05mol?L-1的NaOH溶液500mL,有以下仪器: