题目内容
具有双核10个电子的共价化合物的化学式是 ,
三核10个电子的 共价化合物的化学式是 ,
四核10个电子的共价化合物的化学式是 ,
五核10个电子的共价化合物的化学式是 ,
以上四种化合物的热稳定性由小到大的顺序是 .
三核10个电子的 共价化合物的化学式是
四核10个电子的共价化合物的化学式是
五核10个电子的共价化合物的化学式是
以上四种化合物的热稳定性由小到大的顺序是
考点:质子数、中子数、核外电子数及其相互联系,分子、原子、离子
专题:原子组成与结构专题
分析:熟悉常见10电子微粒:(加*的是不太常用的)
一核:Ne、*N3-、O2-、F-、Na+、Mg2+、Al3+
二核:HF、OH-
三核:H2O、*NH2-
四核:NH3、H3O+
五核:CH4、NH4+
元素的非金属性越强其氢化物越稳定.
一核:Ne、*N3-、O2-、F-、Na+、Mg2+、Al3+
二核:HF、OH-
三核:H2O、*NH2-
四核:NH3、H3O+
五核:CH4、NH4+
元素的非金属性越强其氢化物越稳定.
解答:
解:具有双核10个电子的共价化合物的化学式是HF,
三核10个电子的共价化合物的化学式是H2O;
四核10个电子的共价化合物的化学式是NH3,
五核10个电子的共价化合物的化学式是CH4,
非金属性强弱顺序是F>O>N>C,所以其热稳定性由强到弱的顺序是HF>H2O>NH3>CH4,
故答案为:HF;H2O;NH3;CH4;HF>H2O>NH3>CH4.
三核10个电子的共价化合物的化学式是H2O;
四核10个电子的共价化合物的化学式是NH3,
五核10个电子的共价化合物的化学式是CH4,
非金属性强弱顺序是F>O>N>C,所以其热稳定性由强到弱的顺序是HF>H2O>NH3>CH4,
故答案为:HF;H2O;NH3;CH4;HF>H2O>NH3>CH4.
点评:本题主要考查了常见的10电子微粒以及元素周期律的运用,难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
下列物质性质的变化规律与共价键无关的是( )
| A、HF、HCl、HBr、HI的热稳定性依次减弱 |
| B、金刚石的硬度大于硅,其熔、沸点也高于硅 |
| C、NaF、NaCl、NaBr、NaI的熔点依次降低 |
| D、F2、Cl2、Br2、I2的键能逐渐减小 |
现有一多肽,其化学式为C60H77O22N11,将其彻底水解后只得到下列四种氨基酸:甘氨酸(H2N-CH2COOH),苯丙氨酸(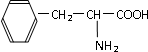 ),丙氨酸,谷氨酸,则该多肽中所含肽键的数目以及水解后得到的谷氨酸苯丙氨酸的数目分别是( )
),丙氨酸,谷氨酸,则该多肽中所含肽键的数目以及水解后得到的谷氨酸苯丙氨酸的数目分别是( )
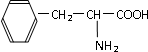 ),丙氨酸,谷氨酸,则该多肽中所含肽键的数目以及水解后得到的谷氨酸苯丙氨酸的数目分别是( )
),丙氨酸,谷氨酸,则该多肽中所含肽键的数目以及水解后得到的谷氨酸苯丙氨酸的数目分别是( )| A、11,4,3 |
| B、11,5,3 |
| C、10,5,3 |
| D、10,4,3 |
下列有机物中属于醇的是( )
A、 |
B、 |
| C、CH3OCH3 |
D、 |
 ,某有机物X的键线式为:
,某有机物X的键线式为:
 (1)化学式为C6H12的某烃的所有碳原子都在同一平面上,则该烃的结构简式为
(1)化学式为C6H12的某烃的所有碳原子都在同一平面上,则该烃的结构简式为