题目内容
配制100ml 1.0mol/L CuSO4溶液,求:
①用无水硫酸铜配制,则需CuSO4的质量?
②用胆矾配制,则需CuSO4?5H2O的质量?
③用5.0mol/L CuSO4溶液加水稀释配制,则需5.0mol/L CuSO4溶液多少毫升.
①用无水硫酸铜配制,则需CuSO4的质量?
②用胆矾配制,则需CuSO4?5H2O的质量?
③用5.0mol/L CuSO4溶液加水稀释配制,则需5.0mol/L CuSO4溶液多少毫升.
考点:物质的量浓度的相关计算
专题:计算题
分析:首先根据n=cV计算100ml 1.0mol/L CuSO4溶液中CuSO4的物质的量,根据m=nM计算溶质的质量,根据溶液稀释前后溶质的物质的量不变计算所需溶液的体积.
解答:
解:配制100ml 1.0mol/L CuSO4溶液,需要硫酸铜的物质的量为:n(CuSO4)=0.1L×1.0mol/L=0.1mol,则
①用无水硫酸铜配制,则需CuSO4的质量为:m(CuSO4)=0.1mol×160g/mol=16g,
答:需要无水硫酸铜粉末的质量是16g;
②m(CuSO4?5H2O)=0.1mol×250g/mol=25g,
答:需要胆矾的质量是25g;
③溶液稀释前后溶质的物质的量不变,设需要5.0mol/L CuSO4溶液的体积为V,则有
0.1L×1.0mol/L=V×5.0mol/L,
V=0.02L=20mL,
答:若用5.0mol/L CuSO4溶液配制,则需要该溶液20mL.
①用无水硫酸铜配制,则需CuSO4的质量为:m(CuSO4)=0.1mol×160g/mol=16g,
答:需要无水硫酸铜粉末的质量是16g;
②m(CuSO4?5H2O)=0.1mol×250g/mol=25g,
答:需要胆矾的质量是25g;
③溶液稀释前后溶质的物质的量不变,设需要5.0mol/L CuSO4溶液的体积为V,则有
0.1L×1.0mol/L=V×5.0mol/L,
V=0.02L=20mL,
答:若用5.0mol/L CuSO4溶液配制,则需要该溶液20mL.
点评:本题考查物质的量浓度的计算,题目难度中等,注意相关计算公式的运用,特别是溶液稀释前后溶质的物质的量不变,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
几种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是( )
| 元素代号 | L | X | R | T |
| 原子半径/nm | 0.191 | 0.102 | 0.154 | 0.074 |
| 主要化合价 | +1 | +6、-2 | +1 | -2 |
| A、L单质的熔点比R单质的高 |
| B、T对应的氢化物的沸点比X对应的氢化物高 |
| C、R单质在氧气中燃烧生成R2O2 |
| D、L、X形成的简单离子核外电子数相等 |
只用滴管、试管和水就能鉴别的物质组是( )
| A、苯、乙酸、CCl4 |
| B、乙醇、乙醛、乙酸 |
| C、乙二醇、乙醛、溴代烃 |
| D、乙醇、甘油、苯酚 |
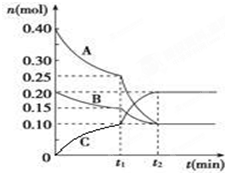 现将0.4mol A气体和0.2mol B气体充入10L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量随时间的变化如图:
现将0.4mol A气体和0.2mol B气体充入10L的密闭容器中,在一定条件下使其发生反应生成气体C,其物质的量随时间的变化如图: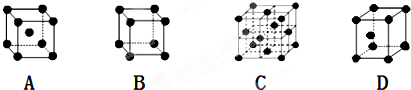
 是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为
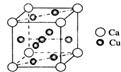
是金属Ca和Cu所形成的某种合金的晶胞结构示意图,则该合金中Ca和Cu的原子个数比为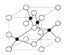 是铜的某种氧化物的晶胞结构示意图,该晶体的密度为a g/cm3,设阿伏伽德罗常数的值为NA,则该晶胞的体积为
是铜的某种氧化物的晶胞结构示意图,该晶体的密度为a g/cm3,设阿伏伽德罗常数的值为NA,则该晶胞的体积为