题目内容
20.为了高效解决化石燃料燃烧存在的问题,不需要研究的问题有( )| A. | 杜绝化石燃料的使用,从源头上解决问题 | |
| B. | 减少燃料燃烧产生的热量损耗的技术,提高燃料利用率的措施 | |
| C. | 防止燃料燃烧造成环境污染的方法 | |
| D. | 通过化学方法把化石燃料转化成洁净燃料 |
分析 A.化石燃料是重要的能源;
B.提高燃料利用率可以节约能源;
C.化石燃料燃烧会产生大气污染;
D.把化石燃料转化成洁净燃料可以减少有害物质的排放.
解答 解:A.化石燃料是重要的能源,也是重要的工业原料,不可能完全杜绝化石燃烧的使用,故A选;
B.减少燃料燃烧产生的热量损耗的技术,提高燃料利用率可以节约能源,能减少燃烧产物的排放,减轻大气污染,是需要研究的问题,故B不选;
C.化石燃料燃烧会产生大气污染,研究防止燃料燃烧造成环境污染的方法,能高效解决化石燃料燃烧存在的问题,故C不选;
D.把化石燃料转化成洁净燃料,有利于燃料的充分燃烧,能提高燃料利用率,可以减少有害物质的排放,是需要研究的问题,故D不选.
故选A.
点评 本题考查能源以及环境污染和治理,侧重于化学与人体健康的考查,为高考常见题型和高频考点,有利于培养学生的良好科学素养,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
20.下列有机分子中,所有原子不可能处在同一平面上的是( )
| A. | 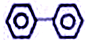 | B. | 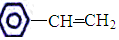 | C. |  | D. | 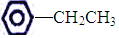 |
11.分子式为C9H11Cl且含有苯环的同分异构体数目为( )
| A. | 30 | B. | 36 | C. | 39 | D. | 42 |
15.下列物质间的归类正确的是( )
| A. | 1H、2H、3H互为同素异形体 | |
| B. | 碳酸氢钠和纯碱是同一物质 | |
| C. | 乙醇(CH3CH2OH)与甲醚(CH3OCH3)互为同分异构体 | |
| D. | O2与O3互为同位素 |
5.表是某城市空气质量每周公报的部分内容.下列选项中不会对表中3个空气质量指标产生影响的是( )
| 项目 | 空气污染指数(API) | 空气质量级别 | 空气质量描述 |
| 总悬浮颗粒 | 52 | Ⅱ | 良 |
| 二氧化硫 | 7 | I | 优 |
| 二氧化氮 | 24 | I | 优 |
| A. | 用煤和石油产品作燃料 | B. | 汽车排放的尾气 | ||
| C. | 使用含磷洗衣粉 | D. | 焚烧垃圾 |
12.从键长的角度来判断下列共价键中最稳定的是( )
| A. | H-F | B. | H-N | C. | H-C | D. | H-S |
9.草酸钴用途广泛,可用于指示剂和催化剂的制备.一种利用水钴矿制取草酸钴晶体(CoC2O4?2H2O)工艺流程如图1:
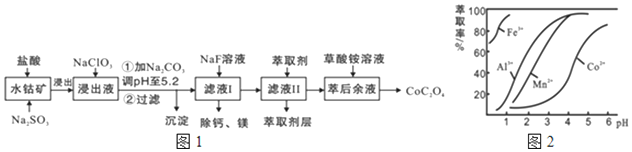
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)浸出过程中加入Na2SO3的 离子方程式为2Co3++SO32-+H2O=2Co2++SO42-+2H+
(2)NaClO3的作用是将Fe2+氧化为Fe3+; 调PH至5.2,沉淀的主要成分为Al(OH)3、Fe(OH)3
(3)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是除去Mn2+;使用萃取剂适宜的pH是B
A.接近2.0 B.接近3.0 C.接近5.0
(4)除钙、镁是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀,已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+):c(Ca2+)=0.7.
(5)已知含钴废料中含Co2O3质量分数为a%,若取mkg该含钴废料按照上述流程,理论上最多能制得草酸钴晶体的质量为$\frac{1830ma}{83}$或16.6mag.

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的PH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3的作用是将Fe2+氧化为Fe3+; 调PH至5.2,沉淀的主要成分为Al(OH)3、Fe(OH)3
(3)萃取剂对金属离子的萃取率与pH的关系如图2所示.滤液Ⅱ中加入萃取剂的作用是除去Mn2+;使用萃取剂适宜的pH是B
A.接近2.0 B.接近3.0 C.接近5.0
(4)除钙、镁是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀,已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+):c(Ca2+)=0.7.
(5)已知含钴废料中含Co2O3质量分数为a%,若取mkg该含钴废料按照上述流程,理论上最多能制得草酸钴晶体的质量为$\frac{1830ma}{83}$或16.6mag.
1.根据元素所在元素周期表的位置,判断下列元素都能作为半导体材料的是( )
| A. | S、K | B. | C、Al | C. | Si、Ge | D. | Ag、Cu |
 .
.