题目内容
8.用两根铂丝做电极插入KOH溶液中,再向两个电极上分别通甲烷气和氧气可形成原电池--燃料电池,根据两极反应的实质判断,通甲烷气的一极电极反应式为:CH4+100H--8e-=CO32-+7H2O,通氧气的一极,在下列叙述中正确的是( )| A. | 阴极:4H2O+2O2-8e-═8OH- | B. | 正极:4H2O+2O2+8e-═8OH- | ||
| C. | 阴极:4OH-+4e-═2H2O+O2↑ | D. | 正极:4OH--4e-═2H2O+O2↑ |
分析 燃料电池中,负极上通入燃料,燃料失电子发生氧化反应,正极上通入氧化剂,氧化剂得电子发生还原反应,该燃料电池为碱性电池,正极上氧气得电子和水反应生成氢氧根离子.
解答 解:燃料电池中,负极上通入燃料,燃料失电子发生氧化反应,正极上通入氧化剂,氧化剂得电子发生还原反应,该燃料电池为碱性电池,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为4H2O+2O2+8e-═8OH-,
故选B.
点评 本题考查电极反应式的书写,为高频考点,明确各个电极上发生的反应是解本题关键,注意结合电解质溶液酸碱性书写,电极反应式的书写为易错点.

练习册系列答案
相关题目
18.从柑橘中可提炼出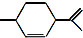 下列关于它的说法不正确的是( )
下列关于它的说法不正确的是( )
 下列关于它的说法不正确的是( )
下列关于它的说法不正确的是( )| A. | 分子式为C10H16 | B. | 其一氯代物有8种 | ||
| C. | 能与溴水发生加成反应 | D. | 常温下呈液态,难溶于水 |
19.下列有关电解质溶液中粒子浓度关系不正确的是( )
| A. | pH=1的NaHSO4溶液:c(H+)=c(SO42-)+c(OH-) | |
| B. | 常温下,将0.1 mol•L-1CH3COOH溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中$\frac{{c({C{H_3}CO{O^-}})}}{{c({C{H_3}COOH})}}$的值增大到原来的10倍 | |
| C. | pH相等的①NH4Cl ②(NH4)2SO4③NH4HSO4溶液中:c(NH4+)大小顺序:①>③>② | |
| D. | 含等物质的量的NaHC2O4和Na2C2O4的溶液:2c(Na+)=3[c(HC2O4-)+c(C2O42-)+c(H2C2O4)] |
16.下列离子方程式书写正确的是( )
| A. | NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-═BaCO3?+2H2O+CO32- | |
| B. | FeCl3溶液与HI溶液反应:2Fe3++2HI═2Fe2++I2+2H+ | |
| C. | 向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色:2AgCl+S2-═Ag2S↓+2Cl- | |
| D. | 石灰石与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O |
13.将质量为a克的铜丝在酒精灯上加热灼烧后,分别插入到下列溶液中,放置片刻,铜丝质量不变的是( )
| A. | 盐酸 | B. | 氢氧化钠 | C. | 无水乙醇 | D. | 石灰水 |
20.下列反应的离子方程式正确的是( )
| A. | 过氧化钠溶于水:2O22-+2H2O═4OH-+O2↑ | |
| B. | 用小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O | |
| C. | 硫酸铜与Ba(OH)2溶液反应:Cu2++2OH-═Cu(OH)2↓ | |
| D. | 碳酸氢钠与少量Ca(OH)2溶液反应:Ca2++2HCO3-+2OH-═CaCO3↓+CO32-+2H2O |
17.下列说法不正确的是( )
| A. | 三氧化二铁可以用来制作油漆 | |
| B. | 可用超纯硅制造的单晶硅来制造计算机的芯片 | |
| C. | 实验室用二氧化锰和浓盐酸共热制取少量氯气 | |
| D. | 氢氧化钠溶液要盛放在磨口玻璃塞的试剂瓶里 |