题目内容
用NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、0.5 mol锌粒与足量盐酸反应产生11.2 L H2 |
| B、标准状况下,11.2 L CCl4所含分子数为0.5NA |
| C、0.1 mol CH4所含氢原子数为0.4NA |
| D、常温常压下,28 g N2中所含原子个数为NA |
考点:阿伏加德罗常数
专题:
分析:A、依据化学方程式定量关系计算生成氢气0.5mol,温度压强不知不能计算气体体积;
B、标准状况四氯化碳不是气体;
C、依据甲烷含有氢原子数计算;
D、依据n=
计算物质的量,结合分子式计算原子数;
B、标准状况四氯化碳不是气体;
C、依据甲烷含有氢原子数计算;
D、依据n=
| m |
| M |
解答:
解:A、依据化学方程式定量关系计算生成氢气0.5mol,温度压强不知不能计算气体体积,故A错误;
B、标准状况四氯化碳不是气体,11.2 L CCl4物质的量不是0.5mol,故B错误;
C、依据甲烷含有氢原子数计算,0.1 mol CH4所含氢原子数为0.4NA,故C正确;
D、依据n=
计算物质的量
=1mol,结合分子式计算原子数为2NA,故D错误;
故选C.
B、标准状况四氯化碳不是气体,11.2 L CCl4物质的量不是0.5mol,故B错误;
C、依据甲烷含有氢原子数计算,0.1 mol CH4所含氢原子数为0.4NA,故C正确;
D、依据n=
| m |
| M |
| 28g |
| 28g/mol |
故选C.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是气体摩尔体积条件分析,物质的量计算微粒数的方法和注意问题,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
表示溶液的酸碱性,科学家提出了酸度(AG)的概念,AG=lg
,则下列叙述正确的是( )
| c(H+) |
| c(OH) |
| A、中性溶液的AG=0 |
| B、常温下0.lmol/L氢氧化钠溶液AG=12 |
| C、酸性溶液的AG<0 |
| D、常温下0.lmol/L盐酸溶液的AG=12 |
下列有关说法正确的是( )
| A、铁表面镀铜时,铜与电源的正极相连,铁与电源的负极相连 |
| B、用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大 |
| C、一定温度下,反应2Mg(s)+CO2(g)=2MgO(s)+C(s)能自发进行,则该反应△H>0 |
| D、SO2(g)+2CO(g)?2CO2(g)+S(l)达到平衡,保持其他条件不变,分离出硫,正反应速率加快,SO2的转化率提高 |
下列说法正确的是( )
| A、22.4L氧气中一定含有6.02×1023个氧分子 |
| B、18g水在标准状况下的体积是22.4L |
| C、标准状况下,20mL NH3与60mL O2所含的分子数之比为1:3 |
| D、金属元素只能存在于阳离子中 |
设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、16g O3与 O2混合物中所含氧原子数为NA |
| B、2.3gNa+中含有的电子数为0.1NA |
| C、在常温常压下11.2L二氧化碳所含的分子数目为0.5NA |
| D、相同质量的两块钠分别变成氧化钠和过氧化钠前者失去的电子数多 |
下列变化过程,属于放热反应的是( )
①水蒸气变成液态水
②酸碱中和反应
③浓H2SO4稀释
④固体NaOH溶于水
⑤H2在Cl2中燃烧
⑥弱酸的电离.
①水蒸气变成液态水
②酸碱中和反应
③浓H2SO4稀释
④固体NaOH溶于水
⑤H2在Cl2中燃烧
⑥弱酸的电离.
| A、②③④⑤ | B、②③④ |
| C、②⑤ | D、①②③④⑤ |
下列电子式正确的是( )
A、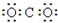 |
B、 |
C、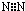 |
D、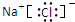 |
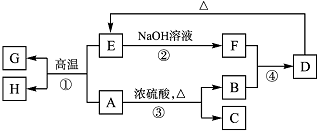 已知A、B、C、D、E、F、G、H可以发生如下图所示的转化(反应过程中部分产物已略去).其中,A、G为同一主族元素的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物.
已知A、B、C、D、E、F、G、H可以发生如下图所示的转化(反应过程中部分产物已略去).其中,A、G为同一主族元素的单质,B、C、H在通常情况下为气体,化合物C是一种形成酸雨的大气污染物.