题目内容
6.下列关于氨气的说法正确的是( )| A. | 氨气可以用浓硫酸干燥也可用碱石灰干燥 | |
| B. | 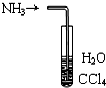 用如图装置吸收NH3可防止倒吸 用如图装置吸收NH3可防止倒吸 | |
| C. | 氨水能导电,所以NH3是电解质 | |
| D. | 氨气可以使湿润的蓝色石蕊试纸变红,依此可检验氨气 |
分析 A.浓硫酸具有酸性,不能干燥碱性气体;
B.氨气极易溶于水,难溶于四氯化碳;
C.氨气本身不能电离;
D.氨气能够使湿润的红色石蕊试纸变蓝.
解答 解:A.氨气为碱性气体,不能用浓硫酸干燥,故A错误;
B.氨气极易溶于水,难溶于四氯化碳,用此装置可以防止氨气被水吸收时发生倒吸,故B正确;
C.氨水能导电是因为氨气与水生成能够电离的电解质一水合氨,但是氨气本身不能电离,所以NH3是非电解质,故C错误;
D.氨气能够使湿润的红色石蕊试纸变蓝,依此可检验氨气,故D错误;
故选:B.
点评 本题考查了氨气的性质,明确氨气为碱性气体、本身不能电离的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
16.部分弱电解质的电离平衡常数如下表:
下列说法不正确的是( )
| 弱电解质 | HCOOH | HCN | H2CO3 | NH3•H2O |
| 电离平衡常数 (25℃) | Ka=1.8×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7Ka2=5.6×10-11 | Kb=1.8×10-5 |
| A. | 结合H+的能力:CO32->CN->HCO3->HCOO- | |
| B. | 0.1mol/L的HCOONH4溶液中:c(HCOO-)>c(NH4+)>c(H+)>c(OH-) | |
| C. | 25℃时,pH=3的盐酸与pH=11的氨水混合,若溶液显中性,则二者消耗的体积是:V(盐酸)>V(氨水) | |
| D. | 0.1mol/L的NaHCO3溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) |
17.下列叙述正确的是( )
| A. | 铜能导电,所以铜是电解质 | |
| B. | BaSO4难溶于水,所以BaSO4属于非电解质 | |
| C. | 虽然液态HCl不能导电,但HCl的水溶液能导电,所以HCl是电解质 | |
| D. | 氯气的水溶液能导电,氯气是电解质 |
14.在光照条件下,等物质的量的甲烷和氯气充分反应,所得取代产物有( )
①CH3Cl ②CH2Cl2 ③CHCl3 ④CCl4.
①CH3Cl ②CH2Cl2 ③CHCl3 ④CCl4.
| A. | 只有① | B. | 只有④ | C. | ①、②和③ | D. | 全部 |
1.下列说法不正确的是( )
| A. | 在船舶的外壳装上镁合金或锌块保护钢铁设备被称为牺牲阳极的阴极保护法 | |
| B. | 赤潮、白色污染、绿色食品中的“赤”“白”“绿”均指相关物质的颜色 | |
| C. | 海水淡化的方法主要有:蒸馏法、电渗析法、离子交换法等 | |
| D. | 乙烯的产量可以用来衡量一个国家的石油化工发展水平 |
18.下列各反应对应的离子方程式正确的是( )
| A. | 向含3mol次氯酸钠溶液中通入1mol二氧化硫:3ClO-+H2O+SO2═2HClO+SO4-+Cl- | |
| B. | 向碳酸氢钠溶液中加入过量氢氧化钙溶液2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| C. | 氢氧化钡溶液与硫酸溶液反应得到中性溶液Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 50mL1mol/L的FeI2溶液中通入0.05molCl2:2Fe2++2I-+2Cl2═2Fe3++I2+4Cl- |
15.物质灼烧时,火焰呈紫色的一定含有( )
| A. | 钾原子 | B. | 钾离子 | C. | 钾元素 | D. | 钾的化合物 |
16.在相同温度下等体积、等物质的量浓度的4种稀溶液:①Na2SO4 ②H2SO3 ③NaHSO3④Na2S,所含带电微粒的数目由多到少的顺序是( )
| A. | ①=④>③=② | B. | ①=④>③>② | C. | ①>④>③>② | D. | ④>①>③>② |

