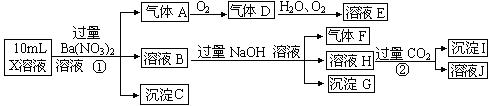
题目内容
13.将等物质的量的Cl2和SO2气体通入BaCl2溶液中,再滴入紫色石蕊溶液,以下叙述正确的是( )| A. | 产生BaSO4白色沉淀,溶液变红色 | B. | 产生BaSO3白色沉淀,溶液变无色 | ||
| C. | 无沉淀产生,溶液变无色 | D. | 产生BaSO4白色沉淀,溶液变无色 |
分析 二氧化硫与氯气等物质的量通入水中发生化学反应:SO2 +Cl2 +2H2O=H2SO4+2HCl,依据生成物硫酸与盐酸的性质判断解答.
解答 解:二氧化硫与氯气等物质的量通入水中发生化学反应:SO2 +Cl2 +2H2O=H2SO4+2HCl,硫酸和氯化氢为强酸,电离产生氢离子,溶液显酸性,能使石蕊变红色,硫酸能够与氯化钡溶液生成硫酸钡白色沉淀,
故选:A.
点评 本题考查了元素化合物性质,明确二氧化硫、氯气的性质是解题关键,题目难度不大.

练习册系列答案
相关题目
4.生活中的一些小常识往往包含化学知识,以下叙述不正确的是( )
| A. | 用食醋清除暖水瓶中的水垢 | |
| B. | 纤维素在人体内可水解为葡萄糖,故可作为人类的营养物质 | |
| C. | 用热的纯碱水洗涤油垢 | |
| D. | 葡萄糖中花青素在碱性环境下显紫色,故可用苏打粉打粉检验假红酒 |
8.在一定温度下,容积一定的密闭容器中发生反应A(s)+2B(g)?C(g)+D(g),当下列物理量不再发生变化时,表明反应已达平衡的是( )
①混合气体的密度
②混合气体的压强
③B的物质的量浓度
④混合气体的总物质的量.
①混合气体的密度
②混合气体的压强
③B的物质的量浓度
④混合气体的总物质的量.
| A. | ①② | B. | ①③ | C. | ②③ | D. | ①④ |
18.将下列溶液分别加入到FeCl3、Al2(SO4)3、Cu(NO3)2、MgCl2和Na2CO3五种溶液中,产生现象种类最多且把五种溶液区别开的是( )
| A. | H2SO4溶液 | B. | BaCl2溶液 | C. | NaOH溶液 | D. | AgNO3溶液 |
5.主族元素X在周期表中位于第二周期,其原子最外层电子数大于4,元素Y在周期表中位于第三周期,其原子最外层电子数小于4,有关其说法正确的是( )
| A. | X所形成的单质都是双原子分子 | |
| B. | 原子半径X>Y | |
| C. | X、Y能形成的阴、阳离子数之比为1:2离子化合物,其一定为碱性氧化物 | |
| D. | 由X、Y组成的某化合物与水反应能生成一种强碱和一种弱碱,其简单离子半径:X>Y |
2.常温下,pH=3的盐酸aL分别与下列3种溶液混合,充分反应后溶液呈中性
①pH=11的氨水bL
②物质的量浓度为1×10-1mol•L-1的氨水cL
③c(OH)=1×10-3mol•L-1的Ba(OH)2溶液dL.
试判断a、b、c、d大小关系正确的为( )
①pH=11的氨水bL
②物质的量浓度为1×10-1mol•L-1的氨水cL
③c(OH)=1×10-3mol•L-1的Ba(OH)2溶液dL.
试判断a、b、c、d大小关系正确的为( )
| A. | c>a=d>b | B. | b>a=d>c | C. | c>a>b>d | D. | a=b>c>d |
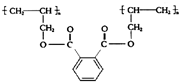 则合成该高聚物的单体的正确组合是( )
则合成该高聚物的单体的正确组合是( )