题目内容
19.铁钉和碳棒用导线连接后,浸入到0.01mol•L-1 NaCl溶液中,可能发生的是( )①碳棒上有氢气析出②碳棒附近产生OH-③发生析氢腐蚀④发生吸氧腐蚀.
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
分析 铁棒与石墨棒用导线连接后浸入0.01mol•L-1的食盐溶液中,构成原电池,Fe为负极,石墨为正极,发生吸氧腐蚀,以此来解答.
解答 解:铁棒与石墨棒用导线连接后浸入0.01mol•L-1的食盐溶液中,构成原电池,Fe为负极,石墨为正极,发生吸氧腐蚀,
①碳棒上氧气得电子生成氢氧根离子,没有氢气析出,故错误;
②碳棒上氧气得电子生成氢氧根离子,即碳棒附近产生OH-,故正确;
③中性条件下,发生吸氧腐蚀,故错误;
④电解质溶液为NaCl溶液,显中性,中性条件下发生吸氧腐蚀,故正确;
故选D.
点评 本题考查了原电池原理和吸氧腐蚀,明确电极的判断及发生的电极反应即可解答,题目难度不大,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
9.在电解质溶液中插入M、N电极,并连接直流电源进行电解,可以看到两极上均有气泡产生,电解后测定电解质溶液,其H+浓度无变化.符合这些条件的是( )
| A. | 两个电极均为铁片,M是阴极,电解质溶液是0.4%的NaOH溶液 | |
| B. | 两个电极均为石墨,M是阳极,电解质溶液是0.4%的H2SO4溶液 | |
| C. | M是铁片,作阴极,N是石墨,电解质溶液是0.4%的Ba(NO3)2溶液 | |
| D. | M是铁片,作阴极,N是石墨,电解质溶液是0.4%的HCl溶液 |
7.BF3与一定量的水形成(H2O)2•BF3晶体Q,Q在一定条件下可转化为R:
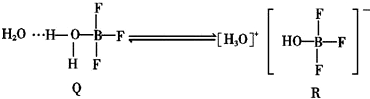
反应过程中新形成的化学键中无( )

反应过程中新形成的化学键中无( )
| A. | 离子键 | B. | 配位键 | C. | 非极性共价键 | D. | 氢键 |
14.茶叶中铁元素的检测可经过以下A、B、C、D四个步骤完成,各步骤中选用的实验仪器不会全部都用上的是( )
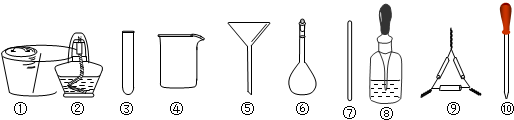

| A. | 将茶叶灼烧灰化,选用①、②和⑨ | |
| B. | 用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦ | |
| C. | 过滤得到滤液,选用④、⑤和⑦ | |
| D. | 检验滤液中的Fe3+,选用③和⑧ |
11.在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应:A(s)+2B(g)?C(g)+D(g)已达到平衡状态的是( )
①混合气体的平均相对分子质量; ②混合气体的密度; ③B的物质的量浓度;
④气体总物质的量; ⑤混合气体的压强 ⑥C、D反应速率的比值.
①混合气体的平均相对分子质量; ②混合气体的密度; ③B的物质的量浓度;
④气体总物质的量; ⑤混合气体的压强 ⑥C、D反应速率的比值.
| A. | ②③⑤ | B. | ②③④⑥ | C. | ①③④⑤ | D. | ①②③ |
9.随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点.
完成下列填空:
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g)?CH4(g)+2H2O(g)
已知H2的体积分数随温度的升高而增加.
若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化.(选填“增大”、“减小”或“不变”)
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
a、b、c、d与m、n、x、y之间的关系式为$\frac{c{d}^{2}}{a{b}^{4}}=\frac{x{y}^{2}}{m{n}^{4}}$.
(3)碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11
草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5
0.1mol/L Na2CO3溶液的pH大于0.1mol/L Na2C2O4溶液的pH.(选填“大于”“小于”或“等于”)
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是草酸.若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是ac.(选填编号)
a.[H+]>[HC2O4-]>[HCO3-]>[CO32-]b.[HCO3-]>[HC2O4-]>[C2O42-]>[CO32-]
c.[H+]>[HC2O4-]>[C2O42-]>[CO32-]d.[H2CO3]>[HCO3-]>[HC2O4-]>[CO32-]
(4)人体血液中的碳酸和碳酸氢盐存在平衡:H++HCO3-?H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象当少量酸性物质进入血液中,平衡向右移动,使H+浓度变化较小,血液中的pH基本不变;当少量碱性物质进入血液中,平衡向左移动,使H+浓度变化较小,血液的pH基本不变.
完成下列填空:
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g)?CH4(g)+2H2O(g)
已知H2的体积分数随温度的升高而增加.
若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化.(选填“增大”、“减小”或“不变”)
| v正 | v逆 | 平衡常数K | 转化率α |
| [CO2]/mol•L-1 | [H2]/mol•L-1 | [CH4]/mol•L-1 | [H2O]/mol•L-1 | |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
(3)碳酸:H2CO3,Ki1=4.3×10-7,Ki2=5.6×10-11
草酸:H2C2O4,Ki1=5.9×10-2,Ki2=6.4×10-5
0.1mol/L Na2CO3溶液的pH大于0.1mol/L Na2C2O4溶液的pH.(选填“大于”“小于”或“等于”)
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是草酸.若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是ac.(选填编号)
a.[H+]>[HC2O4-]>[HCO3-]>[CO32-]b.[HCO3-]>[HC2O4-]>[C2O42-]>[CO32-]
c.[H+]>[HC2O4-]>[C2O42-]>[CO32-]d.[H2CO3]>[HCO3-]>[HC2O4-]>[CO32-]
(4)人体血液中的碳酸和碳酸氢盐存在平衡:H++HCO3-?H2CO3,当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象当少量酸性物质进入血液中,平衡向右移动,使H+浓度变化较小,血液中的pH基本不变;当少量碱性物质进入血液中,平衡向左移动,使H+浓度变化较小,血液的pH基本不变.
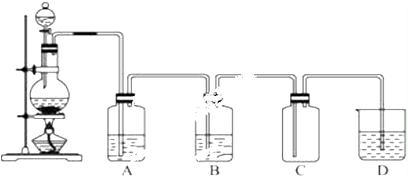
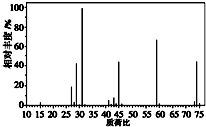 根据以下有关信息确定有机物的组成
根据以下有关信息确定有机物的组成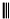 +
+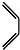 $\stackrel{△}{→}$
$\stackrel{△}{→}$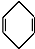 如果要合成
如果要合成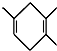 ,所用的起始原料的结构简式为C(CH3)2=C(CH3)2、CH3C≡CH或CH2=C(CH3)-CH=CH2、CH3C≡CCH3.
,所用的起始原料的结构简式为C(CH3)2=C(CH3)2、CH3C≡CH或CH2=C(CH3)-CH=CH2、CH3C≡CCH3.
 ;
;