题目内容
7.下列推断正确的是( )| A. | 某物质既能溶于盐酸,又能溶于NaOH溶液,则该物质一定是Al2O3 | |
| B. | 某气体只含C、H两种元素,且质量之比为6:1,则该气体一定为纯净物 | |
| C. | SO2通入品红溶液中,溶液褪色,则SO2通入紫色石蕊试液中,溶液也褪色 | |
| D. | 浓硝酸在光照条件下变黄,说明浓硝酸不稳定,生成的有色产物能溶于浓硝酸 |
分析 A.既能与盐酸反应又能与NaOH溶液反应的物质有Al、Al2O3、Al(OH)3、弱酸酸式盐、弱酸的铵盐、氨基酸等;
B.某气体只含C、H两种元素,且质量之比为6:1,则该物质的通式为CnH2n;
C.SO2不能漂白紫色石蕊溶液;
D.硝酸分解生成二氧化氮,二氧化氮溶解在硝酸中.
解答 解:A.既能与盐酸反应又能与NaOH溶液反应的物质有Al、Al2O3、Al(OH)3、弱酸酸式盐、弱酸的铵盐、氨基酸等,所以某物质既能溶于盐酸,又能溶于NaOH溶液,则该物质不一定是Al2O3,故A错误;
B.某气体只含C、H两种元素,且质量之比为6:1,则该物质的通式为CnH2n,所以可能是一种物质,也可能是多种物质,故B错误
C.SO2不能漂白紫色石蕊溶液,SO2通入紫色石蕊溶液,溶液会变红色,故C错误;
D.硝酸分解生成二氧化氮,二氧化氮溶解在硝酸中,二氧化氮为红棕色,所以硝酸会变黄,故D正确.
故选D.
点评 本题考查了元素化合物的性质,题目难度不大,侧重于基础知识的综合应用的考查,注意把握有机物的通式、二氧化硫的漂白性以及硝酸和二氧化氮的性质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.下列除杂(括号内为杂质)使用的主要实验方法正确的是( )
| A. | NaCl溶液(CaCO3):加热 | B. | NaHCO3溶液(Na2CO3):加热 | ||
| C. | H2O(NaCl):蒸馏 | D. | 苯(水):萃取 |
12.下列有关说法不正确的是( )
| A. | 电解法精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| B. | 铅蓄电池中Pb作负极,PbO2作正极 | |
| C. | 在物质的量浓度相等的NaCl和KBr的混合溶液中滴加AgNO3溶液,先产生淡黄色沉淀 | |
| D. | 常温下,pH=3的盐酸、醋酸分别用水稀释m倍、n倍后pH相同,则m<n |
19.反应SO2+NO2?NO+SO3在容积不变的密闭容器中达到平衡后,在其他条件不变时,向该容器中通入一定量的O2,则平衡( )
| A. | 向正反应方向移动 | B. | 向逆反应方向移动 | ||
| C. | 平衡不发生移动 | D. | 不发生移动,但容器内压强增大 |
16.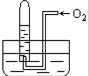 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中,与水充分作用后,试管内水面上升,但不能充满试管,当向试管内鼓如氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的气体可能是( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中,与水充分作用后,试管内水面上升,但不能充满试管,当向试管内鼓如氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的气体可能是( )
 如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中,与水充分作用后,试管内水面上升,但不能充满试管,当向试管内鼓如氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的气体可能是( )
如图所示,试管中盛装的是红棕色气体(可能是混合物),当倒扣在盛有水的水槽中,与水充分作用后,试管内水面上升,但不能充满试管,当向试管内鼓如氧气后,可以观察到试管中水柱继续上升,经过多次重复后,试管内完全被水充满,原来试管中盛装的气体可能是( )| A. | N2与NO2的混和气体 | B. | NO2与O2按4:1体积比混合的气体 | ||
| C. | NO与NO2的混和气体 | D. | NO与O2按4:3体积比混合的气体 |

 HCO3-+H+
HCO3-+H+