题目内容
下列关于35Cl的说法正确的是( )
| A、35Cl2与37Cl2互为同位素 |
B、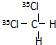 和 和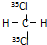 互为同分异构体 互为同分异构体 |
| C、与37Cl的得电子能力相同 |
| D、35Cl-和与它核外电子排布相同的微粒化学性质相同 |
考点:同位素及其应用,分子、原子、离子,同分异构现象和同分异构体
专题:
分析:A.同种元素的不同原子,互称为同位素;
B.分子式相同,结构不同的物质互称为同分异构体;
C.最外层电子数相同,得电子数相同;
D.最外层电子数相同,化学性质相同.
B.分子式相同,结构不同的物质互称为同分异构体;
C.最外层电子数相同,得电子数相同;
D.最外层电子数相同,化学性质相同.
解答:
解:A、两者均是氯气单质,是一种物质,故A错误;
B、甲烷为正四面体结构,其二氯取代物只有一种,故二者是同一种物质,故B错误;
C、两者互为同位素,最外层电子数相同,化学性质相同,故C正确;
D、35Cl-最外层达到了8个电子的稳定结构,化学性质不活泼,氯原子化学性质活泼,故D错误,故选C.
B、甲烷为正四面体结构,其二氯取代物只有一种,故二者是同一种物质,故B错误;
C、两者互为同位素,最外层电子数相同,化学性质相同,故C正确;
D、35Cl-最外层达到了8个电子的稳定结构,化学性质不活泼,氯原子化学性质活泼,故D错误,故选C.
点评:本题考查原子组成和结构,难度不大,注意同种元素的不同原子组成的同种单质化学性质相同.

练习册系列答案
相关题目
 把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )
把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )| A、X为CO2,Y为Ca(OH)2 |
| B、X为NH3?H2O,Y为AlCl3 |
| C、X为NaOH,Y为AlCl3 |
| D、X为HCl,Y为NaAlO3 |
关于常温下0.1mol?L-1醋酸钠溶液,下列说法正确的是( )
| A、水电离出来的c(OH-)=1.0×10-13mol?L-1 |
| B、该溶液的pH<13 |
| C、溶液中离子浓度关系:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D、加入等浓度等体积的盐酸,溶液中:c(CH3COOH)+c(CH3COO-)=c(Cl-)+c(Na+) |
下列表示对应化学反应的离子方程式正确的是( )
| A、Na2O2溶于水产生O2:2O22-+2H2O═O2↑+4OH- |
| B、向氨水通入足量SO2:SO2+2NH3?H2O═2NH4++SO32-+H2O |
| C、次氯酸钠与浓盐酸反应产生Cl2:ClO-+Cl-+H2O═Cl2↑+2OH- |
| D、碳酸氢钠溶液和少量氢氧化钡溶液混合:Ba2++2OH-+2HCO3-═BaCO3↓+CO32-+2H2O |
下列反应的离子方程式不能用H++OH-═H2O表示的是( )
| A、硫酸氢钠和氢氧化钡 |
| B、氢氧化钾和盐酸 |
| C、硝酸和氢氧化钠 |
| D、氢氧化钡和硝酸 |
 在一定条件下,向某一密闭容器中,加入一定量的HI或加入一定量的PCl5,反应达到平衡后,在t时刻改变条件,其反应速率与时间的变化关系均可用右图表示.那么对于不同反应在t时刻改变条件的叙述正确的是( )
在一定条件下,向某一密闭容器中,加入一定量的HI或加入一定量的PCl5,反应达到平衡后,在t时刻改变条件,其反应速率与时间的变化关系均可用右图表示.那么对于不同反应在t时刻改变条件的叙述正确的是( )| A、对于2HI(g)?I2(g)+H2(g)反应,t时刻保持温度和体积不变,再加入一定量的HI |
| B、对于2HI(g)?I2(g)+H2(g)反应,t时刻保持温度和压强不变,再加入一定量的HI |
| C、对于PCl5(g)?PCl3(g)+Cl2(g)反应,t时刻保持温度和体积不变,再加入一定量的PCl5 |
| D、对于PCl5 (g)?PCl3(g)+Cl2(g)反应,t时刻保持温度和压强不变,再加入一定量的PCl3 |
下列实验装置或实验操作中错误的是( )
A、 读取液体体积 |
B、 过滤 |
C、 倾倒液体 |
D、 制取二氧化碳 |
将一定量的Fe粉和S粉混合共热,充分反应后冷却,再加入足量稀硫酸,得标准状况气体11.2L,则原混合物可能的组成是( )
| A、n(Fe)<n(S),总质量等于44g |
| B、n(Fe)>n(S),总质量等于44g |
| C、n(Fe)=n(S),总质量大于44g |
| D、n(Fe)<n(S),总质量大于44g |
