题目内容
 把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )
把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )| A、X为CO2,Y为Ca(OH)2 |
| B、X为NH3?H2O,Y为AlCl3 |
| C、X为NaOH,Y为AlCl3 |
| D、X为HCl,Y为NaAlO3 |
考点:镁、铝的重要化合物,化学方程式的有关计算
专题:几种重要的金属及其化合物
分析:由图可知,将物质X逐渐加入(或滴入)Y溶液中,生成沉淀,当Y溶液反应完后,继续加入物质X,物质X能与沉淀反应而使生成的沉淀溶解,且生成沉淀所需要的X的物质的量与沉淀溶解需要的X的物质的量之比为3:1,据此解答.
解答:
解:A、石灰水中通入二氧化碳,先发生反应Ca(OH)2+CO2═CaCO3↓+H2O,生成CaCO3沉淀,当Ca(OH)2溶液反应完后,再继续通入CO2发生反应CO2+CaCO3+H2O═Ca(HCO3)2沉淀消失,所以前后两个过程CO2的物质的量之比为1:1,故A错误;
B、氢氧化钠溶液中滴入氯化铝溶液,先发生反应Al3++4OH-═AlO2-↓+2H2O,不生成沉淀,当氢氧化钠溶液反应完后,再滴入氯化铝溶液发生反应后发生3AlO2-↓+Al3++6H2O═4Al(OH)3↓+6H2O,生成沉淀溶,所以前后两个过程氯化铝的物质的量之比为3:1,故B错误;
C、氯化铝溶液中加入氢氧化钠溶液中,先发生反应Al3++3OH-═Al(OH)3↓,生成Al(OH)3沉淀,当氯化铝溶液反应完后,再滴入氢氧化钠溶液发生反应Al(OH)3+NaOH═NaAlO2+2H2O沉淀溶解至最后消失,所以前后两个过程氢氧化钠的物质的量之比为3:1,故C正确;
D、偏铝酸钠溶液中加入盐酸,先发生反应AlO2-+H++H2O=Al(OH)3↓,生成Al(OH)3沉淀,当偏铝酸钠溶液反应完后,再继续加入盐酸发生反应Al(OH)3+3H+═Al3++3H2O,沉淀消失,所以前后两个过程HCl的物质的量之比为1:3,故D错误;
故选:C.
B、氢氧化钠溶液中滴入氯化铝溶液,先发生反应Al3++4OH-═AlO2-↓+2H2O,不生成沉淀,当氢氧化钠溶液反应完后,再滴入氯化铝溶液发生反应后发生3AlO2-↓+Al3++6H2O═4Al(OH)3↓+6H2O,生成沉淀溶,所以前后两个过程氯化铝的物质的量之比为3:1,故B错误;
C、氯化铝溶液中加入氢氧化钠溶液中,先发生反应Al3++3OH-═Al(OH)3↓,生成Al(OH)3沉淀,当氯化铝溶液反应完后,再滴入氢氧化钠溶液发生反应Al(OH)3+NaOH═NaAlO2+2H2O沉淀溶解至最后消失,所以前后两个过程氢氧化钠的物质的量之比为3:1,故C正确;
D、偏铝酸钠溶液中加入盐酸,先发生反应AlO2-+H++H2O=Al(OH)3↓,生成Al(OH)3沉淀,当偏铝酸钠溶液反应完后,再继续加入盐酸发生反应Al(OH)3+3H+═Al3++3H2O,沉淀消失,所以前后两个过程HCl的物质的量之比为1:3,故D错误;
故选:C.
点评:本题考查化学反应与图象,难度较大,明确发生的化学反应及反应与图象的对应关系是解答的关键,要求学生有将图象信息转换为化学信息的能力,同时对化学知识必须十分熟练.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
 一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( )
一种新型乙醇电池用磺酸类质子作溶剂,比甲醇电池效率高出32倍.电池总反应为:C2H5OH+3O2=2CO2+3H2O,电池示意图如图.下面对这种电池的说法正确的是( )| A、b极为电池的负极 |
| B、设每个电子所带电量为q库仑,则1mol乙醇被氧化产生12NAq库仑的电量 |
| C、电池工作时电流由a极沿导线经灯泡再到b极 |
| D、电池正极的电极反应为:O2+4e-+2H2O=4OH- |
下列关于有机物的说法正确的是( )
| A、乙醇、乙烷和乙酸都可以与钠反应生成氢气 |
| B、苯、乙醇和乙酸都能发生取代反应 |
| C、乙醇和乙酸都存在碳氧双键 |
| D、石油分馏可获得乙酸、苯及其同系物 |
下列变化可通过一步化学反应实现的是( )
| A、N2→NO2 |
| B、Al2O3→Al(OH)3 |
| C、S→SO3 |
| D、SiO2→SiF4 |
下列关于35Cl的说法正确的是( )
| A、35Cl2与37Cl2互为同位素 |
B、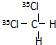 和 和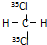 互为同分异构体 互为同分异构体 |
| C、与37Cl的得电子能力相同 |
| D、35Cl-和与它核外电子排布相同的微粒化学性质相同 |
