题目内容
下列各组数据中,前者刚好是后者两倍的是( )
| A、2mol水的摩尔质量和1 mol水的摩尔质量 |
| B、200mL 1 mol/L氯化钙溶液中c(Cl-)和100 mL 1 mol/L氯化钾溶液中c(Cl-) |
| C、64g二氧化硫中的氧原子数和标准状况下22.4L二氧化碳中的氧原子数 |
| D、2mol/LBa(OH)2溶液中Ba2+的物质的量和OH-的物质的量 |
考点:物质的量的相关计算
专题:
分析:A.摩尔质量与物质的量无关;
B.1 mol/L氯化钙溶液中c(Cl-)=2mol/L;1 mol/L氯化钾溶液中c(Cl-)=1mol/L;
C.64g二氧化硫的物质的量为1mol,含有2mol氧原子;标况下22.4L二氧化碳的物质的量为1mol,含有2mol氧原子;
D.氢氧化钡为强电解质,电离方程式Ba(OH)2=Ba2++2OH-.
B.1 mol/L氯化钙溶液中c(Cl-)=2mol/L;1 mol/L氯化钾溶液中c(Cl-)=1mol/L;
C.64g二氧化硫的物质的量为1mol,含有2mol氧原子;标况下22.4L二氧化碳的物质的量为1mol,含有2mol氧原子;
D.氢氧化钡为强电解质,电离方程式Ba(OH)2=Ba2++2OH-.
解答:
解:A.水的摩尔质量为18g/mol,与物质的量多少无关,故A错误;
B.溶液的浓度与体积无关,1 mol/L氯化钙溶液中c(Cl-)=2mol/L;1 mol/L氯化钾溶液中c(Cl-)=1mol/L,故B正确;
C.64g二氧化硫的物质的量为1mol,含有2mol氧原子;标况下22.4L二氧化碳的物质的量为1mol,含有2mol氧原子,前者与后者相等,故C错误;
D.氢氧化钡为强电解质,电离方程式Ba(OH)2=Ba2++2OH-,2mol/LBa(OH)2溶液中Ba2+的物质的量浓度为2mol/L;氢氧根离子的物质的量浓度为4mol/L,二者体积相同,所以Ba2+的物质的量和OH-的物质的量之比为1:2,故D错误;
故选:B.
B.溶液的浓度与体积无关,1 mol/L氯化钙溶液中c(Cl-)=2mol/L;1 mol/L氯化钾溶液中c(Cl-)=1mol/L,故B正确;
C.64g二氧化硫的物质的量为1mol,含有2mol氧原子;标况下22.4L二氧化碳的物质的量为1mol,含有2mol氧原子,前者与后者相等,故C错误;
D.氢氧化钡为强电解质,电离方程式Ba(OH)2=Ba2++2OH-,2mol/LBa(OH)2溶液中Ba2+的物质的量浓度为2mol/L;氢氧根离子的物质的量浓度为4mol/L,二者体积相同,所以Ba2+的物质的量和OH-的物质的量之比为1:2,故D错误;
故选:B.
点评:本题考查了摩尔质量的判断、物质的量浓度及与溶质的质量分数的计算,注意掌握摩尔质量、物质的量浓度概念及计算方法,明确物质的量浓度与溶质质量分数的计算表达式,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列电子式书写正确的是( )
A、溴化铵: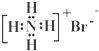 |
B、硫化氢: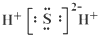 |
C、氮气: |
D、羟基: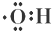 |
使用酸碱中和滴定的方法,用0.1000mo1?L-1盐酸滴定锥形瓶中未知浓度的NaOH溶液,下列操作会使测定结果偏低的是( )
| A、用酸式滴定管量取0.1000 mol?L-1盐酸时,酸式滴定管经蒸馏水洗净后未用0.1000mo1?L-1盐酸润洗 |
| B、滴定前平视读数,滴定结束时俯视读数 |
| C、滴定前滴定管下端尖嘴没有气泡,滴定后读数时发现滴定管下端尖嘴有气泡 |
| D、用未知浓度的Na0H待测液润洗锥形瓶 |
下列有关实验操作说法中,正确的是( )
①用pH试纸测得氯水的pH为2
②用量筒、试管胶头滴管、玻璃棒、蒸馏水和pH试纸,可鉴别pH相等的硫酸和醋酸
③在进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
④用碱式滴定管量取25.00mL溴水
⑤可用渗析的方法除去淀粉中混有的少量NaCl杂质
⑥在进行过滤操作时,为了加快速率,可用玻璃棒不断搅拌过滤器中液体.
①用pH试纸测得氯水的pH为2
②用量筒、试管胶头滴管、玻璃棒、蒸馏水和pH试纸,可鉴别pH相等的硫酸和醋酸
③在进行分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
④用碱式滴定管量取25.00mL溴水
⑤可用渗析的方法除去淀粉中混有的少量NaCl杂质
⑥在进行过滤操作时,为了加快速率,可用玻璃棒不断搅拌过滤器中液体.
| A、①③⑤ | B、②③⑤ |
| C、③④⑤ | D、①③④⑥ |
除去下列溶液中的杂质(括号内是杂质)所用试剂不正确的是( )
| A、KOH溶液[K2CO3]:用Ca(OH)2溶液 |
| B、NaOH溶液[Ba(OH)2]:用Na2SO4溶液 |
| C、NaCl溶液[Na2SO4]:用Ba(NO3)2溶液 |
| D、HNO3溶液[HCl]:用AgNO3溶液 |
下列实验基本操作中不正确的是( )
| A、用量筒量取液体时,视线与量筒内液体凹液面最低处保持水平 |
| B、稀释浓硫酸时,把浓硫酸慢慢倒入盛有水的烧杯中并搅拌 |
| C、用胶头滴管向试管中加入液体时,胶头滴管紧贴试管内壁 |
| D、用托盘天平称量物质时,称量物放在左盘,砝码放在右盘 |
配制0.1mol/L盐酸溶液480mL,用量筒量取密度为1.19g/cm3质量分数为37%的浓盐酸约(取整数)( )mL注入烧杯中.用蒸馏水洗涤烧杯2~3次,将洗涤液注入容量瓶中.
| A、3.5 | B、3.8 |
| C、2.5 | D、4.2 |
下列判断中一定正确的是( )
| A、CaCl2及CaO2固体中阴、阳离子数之比均为2:1 |
| B、等质量的O2与O3中,氧原子的个数比为3:2 |
| C、分别用H2O2、KMnO4分解制O2,当制得等质量O2时,转移电子数之比为1:2 |
| D、10mL 0.3mol?L-1NaCl与30mL0.1mol?L-1AlCl3溶液中Cl-物质的量浓度比为1:3 |
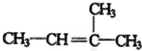 的名称是
的名称是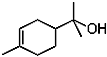 的分子式是
的分子式是