题目内容
配制0.1mol/L盐酸溶液480mL,用量筒量取密度为1.19g/cm3质量分数为37%的浓盐酸约(取整数)( )mL注入烧杯中.用蒸馏水洗涤烧杯2~3次,将洗涤液注入容量瓶中.
| A、3.5 | B、3.8 |
| C、2.5 | D、4.2 |
考点:溶液的配制
专题:计算题
分析:先计算浓盐酸的物质的量浓度,再根据溶液稀释前后溶质的物质的量不变计算所需浓盐酸的体积;
解答:
解:浓盐酸的物质的量浓度c=
=
=11.9mol/L;设需要浓硫酸的体积为V,0.1mol/L×0.5L=11.9mol/L×V,V=0.0042L=4.2mL.用量筒量取密度1.19g/cm3,溶质的质量分数37% 的浓盐酸4.2mL注入烧杯中;
故选D.
| 1000ρω |
| M |
| 1000×1.19×37% |
| 36.5 |
故选D.
点评:本题考查了配制一定浓度的溶液的方法,题目难度中等,注意掌握配制计算浓盐酸的方法.

练习册系列答案
相关题目
下列各组数据中,前者刚好是后者两倍的是( )
| A、2mol水的摩尔质量和1 mol水的摩尔质量 |
| B、200mL 1 mol/L氯化钙溶液中c(Cl-)和100 mL 1 mol/L氯化钾溶液中c(Cl-) |
| C、64g二氧化硫中的氧原子数和标准状况下22.4L二氧化碳中的氧原子数 |
| D、2mol/LBa(OH)2溶液中Ba2+的物质的量和OH-的物质的量 |
对于某些离子的检验及结论一定正确的是( )
| A、取样,加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| B、取样,加入硝酸银有白色沉淀,一定有Cl- |
| C、取样,加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
| D、取样,滴加KSCN溶液,不显红色,再滴加氯水后显红色,一定有Fe2+ |
西维因是一种高效低毒杀虫剂,在碱性条件下可水解:则下列说法正确的是( )
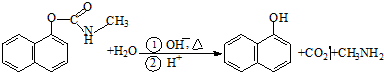

| A、西维因是一种芳香烃 |
| B、西维因分子中所有碳原子一定共面 |
| C、可用FeCl3溶液检验西维因是否发生水解 |
| D、在Ni催化下1mol西维因最多能与6molH2加成 |
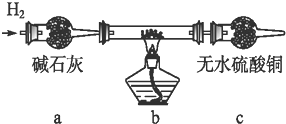 实验结束后,碳棒上的白色物质变为红色,无水硫酸铜不变色.
实验结束后,碳棒上的白色物质变为红色,无水硫酸铜不变色.