题目内容
12.在极性分子中,正电荷重心同负电荷重心间的距离称偶极长,通常用d表示.极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极距(μ)来衡量.分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d•q.试回答以下问题:(1)HCl、CS2、H2S、SO2四种分子中μ=0的是CS2.
(2)对硝基氯苯、邻硝基氯苯、间硝基氯苯,三种分子的偶极矩由大到小的排列顺序是邻>间>对.
(3)实验测得:μ(PF3)=1.03德拜;μ(BCl3)=0.由此可知,PF3分子是三角锥形构型,BCl3分子是平面正三角形构型.
(4)冶癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上.已知该化合物有两种异构体.棕黄色者μ>0,淡黄色者μ=0.试画出两种异形体的构型图.
构型图:淡黄色
 ,棕黄色
,棕黄色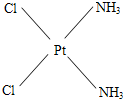 .
.
分析 (1)根据价层电子对互斥模型和题意分析;
(2)偶极矩为偶极长和偶极上一端电荷电量的乘积,即μ=d•q,根据概念判断;
(3)根据分子的极性和结构特点(正负电荷重心是否重合)来思考;
(4)若μ=0,则为非极性分子,NH3和Cl分别对称分布在四边形的4个角上,若μ>0,则为极性分子,NH3和Cl在四边形的4个角上的分布是不对称的.
解答 解:(1)HCl是极性键形成双原子的极性分子.根据价层电子对互斥模型可知,CS2是直线形分子,即非极性分子,其偶极矩为0;H2S、SO2中都是V形,即极性分子,其 μ>0.故 μ=0 的是 CS2,
故答案为:CS2;
(2)分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d•q,对硝基氯苯、邻硝基氯苯、间硝基氯苯,3种分子的d由大到小的排列顺序是:邻>间>对,素以偶极矩关系是邻>间>对,
故答案为:邻>间>对;
(3)μPF3=1.03说明PF3是极性分子,不是非极性分子,即PF3是三角锥形而不是正三角形,μBCl3=0说明 BCl3 是非极性分子,其正负电荷重心重合,应该是平面正三角形.中心原子B与3个Cl原子形成共价键(没有孤对电子),即B的杂化方式是sp2杂化,
故答案为:三角锥形;平面正三角形;
(4)根据题意,Pt(NH3)2Cl2具有平面四边形结构,若μ=0,则为非极性分子,NH3和Cl分别对称分布在四边形的4个角上,即正负电荷重心重合,故淡黄色者是 ;若μ>0,则为极性分子,NH3和Cl在四边形的4个角上的分布是不对称的,即正负电荷重心不重合,故棕黄色者是
;若μ>0,则为极性分子,NH3和Cl在四边形的4个角上的分布是不对称的,即正负电荷重心不重合,故棕黄色者是 ,
,
故答案为: ;
;  .
.
点评 本题考查了简单分子或离子的空间构型,为物质结构与性质模块高频考点.题目难度中等,侧重于新知识的领会及应用能力的培养.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
2.已知某溶液中存在NH4+、Ba2+、Fe3+三种阳离子,则其中可能大量存在的阴离子是( )
| A. | SCN- | B. | CO32- | C. | Cl- | D. | OH- |
3.下列有关有机物的说法正确的是( )
| A. | 甲烷、乙烷、丙烷在光照下分别与氯气反应,生成的一氯代物都只有一种 | |
| B. | 利用减压过滤的方法可以用来快速分离、提纯蛋白质 | |
| C. | 苯与溴水混合,反复振荡后溴水层褪色,这是由于发生了取代反应 | |
| D. | 邻二甲苯只有一种结构,证明苯环中不存在碳碳单键和碳碳双键交替的结构 |
20.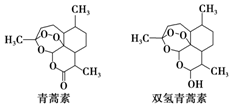 中国科学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素获得2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素的结构式如图.从青蒿中提取青蒿素主要采用有机溶剂提取的方法.下列有关说法不正确的是( )
中国科学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素获得2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素的结构式如图.从青蒿中提取青蒿素主要采用有机溶剂提取的方法.下列有关说法不正确的是( )
 中国科学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素获得2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素的结构式如图.从青蒿中提取青蒿素主要采用有机溶剂提取的方法.下列有关说法不正确的是( )
中国科学家屠呦呦因创制新型抗疟药--青蒿素和双氢青蒿素获得2015年诺贝尔生理学或医学奖.青蒿素和双氢青蒿素的结构式如图.从青蒿中提取青蒿素主要采用有机溶剂提取的方法.下列有关说法不正确的是( )| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 青蒿素通过还原反应可制得双氢青蒿素 | |
| C. | 青蒿素有青蒿的芳香气味,是芳香族化合物 | |
| D. | 用有机溶剂乙醚从青蒿中提取青蒿素,主要采用萃取的方法 |
7.在一定温度下,下列叙述是可逆反应A(g)+3B(g)?2C(g)达平衡时的特征的是( )
(1)单位时间内生成a mol A,同时生成3a mol B;
(2)A、B、C的分子数之比为1:3:2;
(3)单位时间内消耗a mol A,同时生成3a mol B;
(4)A、B、C的浓度不再变化.
(1)单位时间内生成a mol A,同时生成3a mol B;
(2)A、B、C的分子数之比为1:3:2;
(3)单位时间内消耗a mol A,同时生成3a mol B;
(4)A、B、C的浓度不再变化.
| A. | (1)(2) | B. | (3)(4) | C. | (1)(2)(3)(4) | D. | (1)(3) |
17.一定条件下N2(g)+3H2(g)?2NH3(g);△H=-92.4kJ/mol,用1.5molN2和一定量H2反应时,当N2的转化率为80%,达到平衡状态,放出的热量为( )
| A. | 136.8kJ | B. | 110.9kJ | C. | 83.2kJ | D. | 82.4kJ |
1.配制一定物质的量浓度的NaOH溶液时,下列因素会导致溶液浓度偏高的是( )
| A. | 溶解时有少量液体溅出 | B. | 洗涤液未全部转移到容量瓶中 | ||
| C. | 容量瓶使用前未干燥 | D. | 定容时液面未到刻度线 |
2.下列叙述中错误的是( )
| A. | 苯与浓硫酸、浓硝酸共热并保持55~60℃反应生成硝基苯 | |
| B. | 甲苯与氯气在光照的条件下反应主要生成2,4-二氯甲苯 | |
| C. | 苯酚与浓溴水反应生成2,4,6-三溴苯酚 | |
| D. | 丙烯与溴的四氯化碳溶液反应生成1,2-二溴丙烷 |
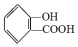 ,
,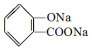 ;请写出将
;请写出将 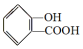 转化为
转化为 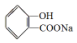 的化学方程式
的化学方程式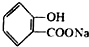 +H2O+CO2↑.
+H2O+CO2↑.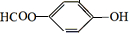
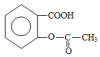 ,它与足量氢氧化钠溶液发生反应的方程式是
,它与足量氢氧化钠溶液发生反应的方程式是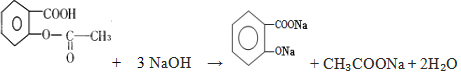 .
.