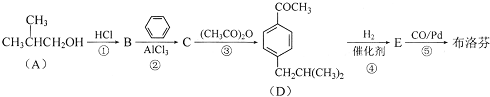
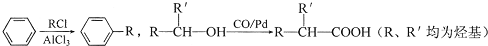题目内容
下列实验操作或说法正确的是( )
| A、配制银氨溶液时是将硝酸银溶液滴入到氨水中至不再生成沉淀为止 |
| B、容量瓶和中和滴定用的锥形瓶用蒸馏水洗净后立即使用,不会对实验结果造成误差 |
| C、检验二氧化硫气体中是否含有二氧化碳,可以将气体通入到饱和碳酸氢钠溶液中 |
| D、为准确测定盐酸与NaOH溶液反应的中和热,所用酸和碱的物质的量应相等 |
考点:化学实验方案的评价
专题:
分析:A.配制银氨溶液时是将稀氨水溶液滴入到硝酸银中至不再生成沉淀为止;
B.量瓶和中和滴定用的锥形瓶用蒸馏水洗净后立即使用,不能用标准液润洗;
C.二氧化硫和碳酸氢钠反应生成二氧化碳;
D.为准确测定盐酸与NaOH溶液反应的中和热,所用酸的物质的量应应该稍微大些.
B.量瓶和中和滴定用的锥形瓶用蒸馏水洗净后立即使用,不能用标准液润洗;
C.二氧化硫和碳酸氢钠反应生成二氧化碳;
D.为准确测定盐酸与NaOH溶液反应的中和热,所用酸的物质的量应应该稍微大些.
解答:
解:A.配制银氨溶液时是将稀氨水溶液滴入到硝酸银中至不再生成沉淀为止,不能将硝酸银滴入氨水中,故A错误;
B.量瓶和中和滴定用的锥形瓶用蒸馏水洗净后立即使用,不能用标准液润洗,否则会产生误差,故B正确;
C.二氧化硫和碳酸氢钠反应生成二氧化碳而干扰二氧化碳的检验,故C错误;
D.为准确测定盐酸与NaOH溶液反应的中和热,盐酸具有挥发性,所用酸的物质的量应应该稍微大些,故D错误;
故选B.
B.量瓶和中和滴定用的锥形瓶用蒸馏水洗净后立即使用,不能用标准液润洗,否则会产生误差,故B正确;
C.二氧化硫和碳酸氢钠反应生成二氧化碳而干扰二氧化碳的检验,故C错误;
D.为准确测定盐酸与NaOH溶液反应的中和热,盐酸具有挥发性,所用酸的物质的量应应该稍微大些,故D错误;
故选B.
点评:本题考查化学实验方案评价,涉及银氨溶液配制、仪器的使用、气体的检验、酸碱中和反应等知识点,明确实验原理是解本题关键,易错选项是D.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是.
| A、硫酸、CuSO4?5H2O、纯碱 |
| B、硫酸氢钠、空气、纯碱 |
| C、氧化铁、明矾、熟石灰 |
| D、硝酸、食盐水、烧碱 |
有关下列实验操作描述不正确的是( )
| A、在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用、环形玻璃搅拌棒进行搅拌、酸和碱正好反应、取2-3 次的实验平均值,以达到良好的实验效果 |
| B、溶质的溶解度越大,溶液的浓度越高,溶剂的蒸发速度越快,溶液的冷却速度越快,析出的晶体就越细小 |
| C、吸滤操作中,吸滤完毕或中途需停止吸滤时,应注意先拆下连接抽气泵和吸滤瓶的橡皮管,然后关闭水龙头,以防倒吸 |
| D、为验证盐桥的作用,在两个烧杯中分别盛适量硫酸亚铁铵溶液稀的酸性高锰酸钾溶液,分别插入石墨棒用导线与电流计相连,然后用装有K2SO4饱和溶液的琼脂的U型管两端插入两个烧杯中,电流计偏转,一段时间后高锰酸钾溶液褪色 |
amolNa2O2和bmolNaHCO3混合置于密闭容器中,加热至300℃使其充分反应.密闭容器内固体为Na2CO3和NaOH混合物时,a和b的比值可能是( )
| A、0.8 | B、1.1 |
| C、1.8 | D、2.2 |
下列关于氯水的叙述,不正确的是( )
| A、在一定浓度的氯水中加小苏打有气泡生成 |
| B、新制氯水中只存在2个平衡状态 |
| C、氯水应保存在棕色瓶中,久置的氯水,PH值减小 |
| D、饱和氯水与石灰石的反应是制取较浓HClO溶液的重要方法 |